
| 被区分的物质 | 区分方法 | |
| A | 烧碱---纯碱 | 各取少量溶液于试管中,分别滴加酚酞试夜,观察颜色变化 |
| B | 硬水---软水 | 各取50ml分别滴加等量肥皂水,搅拌,观察产生泡沫多少 |
| C | 冰----干冰 | 各取一块置于表面皿中,观察有无白雾生成 |
| D | 生石灰---熟石灰 | 各取一药匙分别置于20ml水中,搅拌,测量温度 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据无色酚酞在酸、碱、盐中的显色进行分析;
B、根据肥皂水在硬水和软水中的不同现象进行分析;
C、根据冰是固态的水,干冰是固态的二氧化碳进行分析;
D、根据生石灰与水反应放出大量的热,而熟石灰溶于水温度基本不变进行分析.
解答 解:A、碳酸钠溶液显碱性,能使无色酚酞变红色,氢氧化钠是碱,也能使无色酚酞变红色,现象相同,不能鉴别,故方法错误;
B、各取50mL样品分别滴加等量肥皂水,搅拌,产生泡沫多的是软水,产生泡沫少的是硬水,现象不同,可以鉴别,故方法正确;
C、把冰和干冰露置,产生明显白雾且无液体出现的是干冰,而能融化成液体的是冰,现象不同,可以鉴别,故方法正确;
D、氧化钙和水反应生成氢氧化钙会放出大量的热,氢氧化钙溶于水温度基本不变,取样品溶于水,溶液温度明显升高的是氧化钙,溶液温度基本不变的是氢氧化钙,现象不同,可以鉴别,故方法正确;
故选:A.
点评 本题考查了常见物质的鉴别,在解此类题时,首先分析被鉴别物质的性质,然后选择适当的试剂和方法,出现不同的现象即可鉴别.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  蒙城牛肉 | B. |  涡阳苔干 | C. |  泾县香菜 | D. |  黄山烧饼 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 将该金属丝用砂纸打磨至光亮,加入到装有热水的试管中,并将燃着的小木条放在试管口 | 有气泡不断冒出,气体燃烧,听见爆鸣声,火焰呈淡蓝色 | 生成的气体为_H2 (填化学式) |
| 在反应后的溶液中滴加酚酞溶液 | 溶液变成红色,冷却后红色褪去 | 反应生成了Mg(OH)2,滴加酚酞溶液,溶液变为红色,说明溶液显碱 性 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 通过化学启蒙学习,同学们对组成万物的基本物质有了进一步的了解.
通过化学启蒙学习,同学们对组成万物的基本物质有了进一步的了解.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
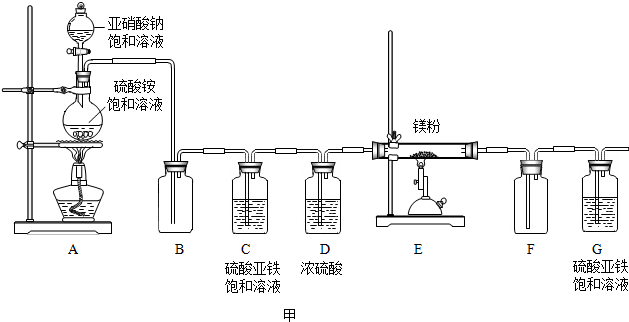
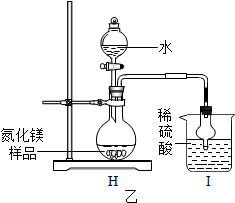
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 单宁酸由碳、氢、氧三种元素组成 | |
| B. | 一个单宁酸分子中含26个氢分子 | |
| C. | 单宁酸分子中碳、氢、氧原子个数比为38:26:23 | |
| D. | 单宁酸中碳元素的质量分数最大 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 用如图装置来测定空气中氧气的含量,下列做法会使实验结果不准确的是( )
用如图装置来测定空气中氧气的含量,下列做法会使实验结果不准确的是( )| A. | 事先在集气瓶内加少量水 | |
| B. | 实验前,检查装置的气密性 | |
| C. | 红磷熄灭后,立即打开弹簧夹 | |
| D. | 该实验可将红磷换成硫粉,烧杯中的水换成浓氢氧化钠溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com