
| 大米种类 | A | B | C | D | E |
| 实验前质量(克) | 20.00 | 20.00 | 20.00 | 20.00 | 20.00 |
| 烘干后质量(克) | 18.00 | 17.00 | 17.50 | 17.40 | 17.80 |
| 大米种类 | A | B | C | D | E |
| 发霉时间(天) | 没有霉变 | 15 | 30 | 35 | 39 |
分析 (1)根据表格数据进行计算;
(2)大米霉变的快慢与含水量有关;
(3)科学探究过程中,进行实验时必须遵循的原则有:对照实验原则和单一变量原则.
(4)利用食物腐败变质是由于微生物的生长和大量繁殖而引起的.根据食物腐败变质的原因,食品保存就要尽量的杀死或抑制微生物的生长和大量繁殖,传统的食品保存方法有风干、盐渍、糖渍、烟熏、酒泡等.现代的贮存方法主要有罐藏、脱水、冷冻、真空包装、添加防腐剂等.
(5)氧化钙和水反应生成氢氧化钙,从而达到延长大米保存时间目的.
解答 解:(1)按照国家对大米含水量的标准14.5%来衡量,五种大米中不合格的是B,其含水量为15%.
(2)根据以上数据,可以得出的结论是:大米霉变的快慢与含水量有关.
(3)小金的实验还不够严谨,除温度与相对湿度外,变量控制上还存在的不足有:没有控制大米的种类,因为不同种类的大米其含有的物质不同.
(4)为了延长大米保存时间,小金发明了新的大米包装袋,将氧化钙包与大米同时密封包装.其主要原理是利用了氧化钙易吸收水分,用化学方程式表示:CaO+H2O═Ca(OH)2.
(5)除(4)方法外,还可采取冷藏、真空保存措施防止大米发霉.
故答案为:(1)B;
(2)大米霉变的快慢与含水量有关;
(3)没有控制大米的种类;
(4)CaO+H2O═Ca(OH)2;
(5)冷藏、真空保存.
点评 解题的关键是知道探究实验的原则和食物保存的方法等.


科目:初中化学 来源: 题型:选择题
| A. | AgNO3→MgCl2 | B. | KNO3→MgCl2 | C. | NaCl→MgCl2 | D. | Mg(OH)2→MgCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 单质 | B. | 原子 | C. | 分子 | D. | 元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
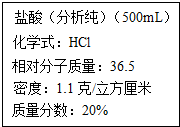 某学校实验室从化学试剂商店买回的一瓶未开封的盐酸试剂(氯化氢水溶液),试剂瓶的标签上的部分内容如图,请仔细阅读后计算
某学校实验室从化学试剂商店买回的一瓶未开封的盐酸试剂(氯化氢水溶液),试剂瓶的标签上的部分内容如图,请仔细阅读后计算查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com