
【题目】推理是化学学习中常见的思维方法。下列推理正确的是( )
A. 红磷和白磷都是由磷元素组成的,所以二者的性质相同
B. 酸能使石蕊试液变红,![]() 也能使紫色的石蕊试液变红,所以
也能使紫色的石蕊试液变红,所以![]() 是酸
是酸
C. 置换反应的生成物是单质和化合物,有单质和化合物生成的反应一定是置换反应
D. 镁粉与盐酸反应放出热量,证明化学反应不仅生成新物质还伴随能量的变化
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:初中化学 来源: 题型:
【题目】2019年5月,187个国家签署了限制塑料废物交易协定,应对“白色污染”挑战。已知某种塑料的组成元素中有碳、氢两种元素,还可能有氧、氯元素中的一种或两种。为了测定其组成,某化学兴趣小组进行如下的探究。
(查阅资料)①无水氯化钙固体可做干燥剂;②有机物中的氯元素燃烧后通常转化为氯化氢。
(设计实验)兴趣小组设计并进行了如图所示的实验。(装置气密性良好)
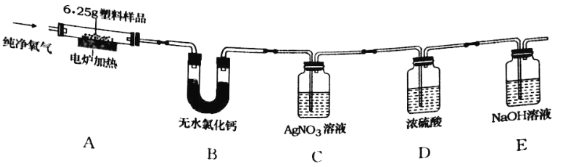
实验过程中,在装置C中观察到________现象,证明该塑料样品中含有氯元素,该反应的化学方程式是________。
(记录数据)6.25g样品在A装置中充分燃烧,反应产物被完全吸收后,测得相关实验数据如表。
装置 | B | C | D | E |
反应后装置增加的质量/g | 1.80 | 3.65 | 0.09 | 8.80 |
(分析与结论)根据以上数据分析与计算,6.25g样品中氢元素的质量为________g,该塑料样品的组成元素是________。
(反思评价)电炉加热前要先通一会儿氧气,目的是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类生活离不开金属.
(1)铁是生活中常用的金属.如图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.

①发热剂需接触到空气才会发热,原因是铁要与 、 等物质共同作用才会生锈.
②推测发热剂成分中氯化钠的作用是 .
(2)应用金属活动性顺序能帮助我们进一步学习金属性质.已知下列各组物质间均能发生置换反应.
A.Fe和CuSO4溶液 B.Mg和MnSO4溶液 C.Mn和FeSO4溶液
①写出Fe和CuSO4溶液反应的化学方程式 .
②Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】 A和C都是常见的黑色粉末,A、B、E中含有同一元素,红色固体 D能发生如下转化:
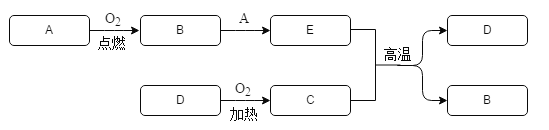
(1)则A是_____,C是_____,D是_____。
(2)写出下列反应的化学方程式:A+B→E:_____;C+E→D+B:_____。该反应属于_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示实验,回答下列问题。

(1)A中实验可得出关于空气中氧气含量的结论是_____。
(2)B中过滤后,滤液仍然浑浊可能的原因是_____(答一点即可)。
(3)C中两支试管内产生气泡速度不同,由此可知影响过氧化氢分解速率的因素是_____。
(4)D中溶液由红色变成无色时,溶液中溶质的组成最多有_____种情况。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置图回答问题:
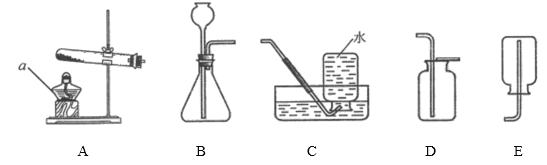
①写出仪器a的名称:________。
②实验室用装置A制氧气,该反应的化学方程式为________。
③实验室用B装置制氢气,药品为锌和稀硫酸,该反应的化学方程式为________,收集氢气应选用的装置为________。
④实验室制二氧化碳的化学方程式为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据图中的信息回答下列问题:
(1)纳米铜在室温下可拉长50多倍而不出现裂纹,说明纳米铜具有:________性质。
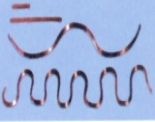
(2)用具有__________性质的高分子薄膜做的鸟笼,可以使鸟和鱼共同生活在水面以下。

(3)检查装置气密性的方法是___________。
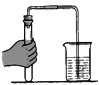
(4)请发挥你的想象写出医用注射器可代替__________化学仪器(答出一种即可)
![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究。
(产品与原理)该厂采用“侯氏制碱法”生产化工产品——纯碱(Na2CO3)和化肥NH4Cl。
生产原理是:将NH3和CO2通入饱和食盐水中得到NaHCO3和NH4Cl的混合物,反应为:NaCl(饱和)+ NH3 + CO2 + H2O = NaHCO3↓+ NH4Cl;分离出NaHCO3晶体,加热制得纯碱。
(生产流程)

(相关资料)
(1) NH4Cl ![]() NH3↑+HCl↑
NH3↑+HCl↑
(2) 已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解的气体体积)
物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
(问题讨论):
(1)氨碱工业最关键的一步是:在加压的条件下不断向饱和的氨盐水中通入二氧化碳气体,溶液中会有碳酸氢钠晶体析出。试分析该流程需要加压条件的原因是:________。流程中加入过量氢氧化钠目的是________。操作II的名称叫________。
(2)反应①中发生了两个反应,写出其中的一个化学方程式:________________。
(3)反应③中得到纯碱的化学方程式为:_________________________________。
(4)上述生产流程中可循环使用的是________(填序号)。
A 气体C B 溶液D C 氢氧化镁 D 化肥NH4Cl
(5)在氨碱工业处理剩余的氯化铵溶液时。为何不直接蒸发结晶析出氯化铵固体?_________。
(组成确定)
(1)称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化。
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀。由上述实验可确定纯碱样品含有杂质________(写化学式)。
(3)某研究性学习小组对刚生产出的纯碱产品进行检测。取22克该样品于烧杯中,加水将其溶解,然后逐滴加入溶质质量分数为14.6%的稀盐酸并不断振荡。
首先发生的反应是:Na2CO3+HCl=NaHCO3+NaCl;然后发生的反应是:NaHCO3+HCl= NaCl+H2O+CO2↑;
在上述过程中烧杯中溶液质量与加入稀盐酸质量的关系如图甲所示。

请你根据图甲提供的信息,计算出反应产生的二氧化碳的质量________;计算该样品中纯碱的质量分数________(计算结果用百分数表示,保留到小数点后一位)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】关于蜡烛的实验探究:小敏是某班的小小化学家,最近对蜡烛产生了兴趣,于是开始了系列实验.
(1)点燃一支蜡烛,先用一木筷迅速插入蜡烛火焰中,片刻后取出,观察到木筷表面出现了如图(a)上所示的圆弧状焦黑斑,其产生的原因是_____。
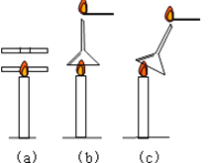
(2)如图(b),在火焰正上方罩一个普通漏斗,用一燃着的火柴接近漏斗颈口处,可观察到火焰____________,是由于____________________。(c)斜插入蜡烛焰心时,观察到漏斗颈口处产生了黄色火焰,这是由于____________。
(3)为了探究蜡烛的燃烧产物,他取了个干冷的小烧杯罩在火焰上方,发现杯壁有____________出现,将小烧杯迅速置,倒入澄清石灰水,振荡,发现石灰水______________,据此他得出蜡烛燃烧生成水和二氧化碳。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com