
科目:初中化学 来源: 题型:选择题
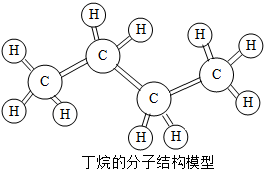 液化石油气是经加压后到钢瓶中的,瓶内压强是大气压强的7-8倍,液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等.下列有关与丁烷的叙述正确的是( )
液化石油气是经加压后到钢瓶中的,瓶内压强是大气压强的7-8倍,液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等.下列有关与丁烷的叙述正确的是( )| A. | 丁烷中碳、氢元素的个数比为2:5 | B. | 丁烷分子中氢元素的质量分数最大 | ||
| C. | 丁烷是由碳、氢原子构成的 | D. | 在通常状况下,丁烷是气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
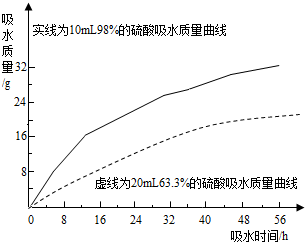 硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:
硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 钢铁是我们日常生活中使用最广泛的金属材料之一.
钢铁是我们日常生活中使用最广泛的金属材料之一.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量滤液于试管中,向其中滴加2-3滴无色酚酞试液,振荡 | 溶液由无色变为红色 | 该瓶中白色粉末一定不是碳酸钙和氯化钠 |
| (2)另取少量滤液于试管中,滴加过量氯化钙溶液,振荡,静置 | 产生白色沉淀 | 该瓶中白色粉末一定有碳酸钠,涉及的化学方程式为Na2CO3+CaCl2=2NaCl+CaCO3↓. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 金属氧化物 | B. | 有机物 | C. | 非金属氧化物 | D. | 盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 探究氯酸钾和二氧化锰制氧气实验中反应物与催化剂的最佳质量比.实验中采用右图实验装置,取20g氯酸钾,分成10等份,每份2g,分别装入10支试管中.在10支试管中分别加入不同质量的二氧化锰,分别测量二氧化锰与氯酸钾在不同质量比时,生成200ml氧气所消耗的时间.实验记录的数据如下:
探究氯酸钾和二氧化锰制氧气实验中反应物与催化剂的最佳质量比.实验中采用右图实验装置,取20g氯酸钾,分成10等份,每份2g,分别装入10支试管中.在10支试管中分别加入不同质量的二氧化锰,分别测量二氧化锰与氯酸钾在不同质量比时,生成200ml氧气所消耗的时间.实验记录的数据如下:| 实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 二氧化锰的质量(g) | 0.1 | 0.2 | 0.33 | 0.4 | 0.5 | 0.66 | 1 | 1.3 | 2 | 3 |
| 二氧化锰与氯酸钾的质量比 | 1:20 | 1:10 | 1:6 | 1:5 | 1:4 | 1:3 | 1:2 | 2:3 | 1:1 | 3:2 |
| 生成200mL氧气时间(秒) | 235 | 186 | 162 | 147 | 133 | 117 | 143 | 160 | 211 | 244 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 两会时“实名制”矿泉水亮相,服务员们“沏茶倒水”的场景不再出现,取而代之的是为每名委员提供一瓶矿泉水,而且每瓶矿泉水上还贴有委员名字.相关说法不正确的是( )
两会时“实名制”矿泉水亮相,服务员们“沏茶倒水”的场景不再出现,取而代之的是为每名委员提供一瓶矿泉水,而且每瓶矿泉水上还贴有委员名字.相关说法不正确的是( )| A. | 矿泉水属于溶液 | |
| B. | 水是人体六大类营养物质之一 | |
| C. | 矿泉水中的矿物质钙、锌、铁、硒都属于人体需要的微量元素 | |
| D. | 灌装矿泉水的塑料瓶子由聚乙烯材料制作而成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com