

 、
、 、
、 分别表示N2、H2、NH3.在催化剂表面(下图中
分别表示N2、H2、NH3.在催化剂表面(下图中 表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:

 ×100%=14g.
×100%=14g. ×100%)=3.08g;
×100%)=3.08g; ×100%=18.1%,所以该奶粉包装袋上所注蛋白质的含量不真实;
×100%=18.1%,所以该奶粉包装袋上所注蛋白质的含量不真实; ×100%)=3.08g;
×100%)=3.08g; ×100%=18.1%,所以该奶粉包装袋上所注蛋白质的含量不真实.
×100%=18.1%,所以该奶粉包装袋上所注蛋白质的含量不真实.

 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:初中化学 来源: 题型:
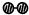 、
、 、
、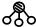 分别表示N2、H2、NH3.观察下图,写出符合在催化剂表面合成氨反应过程的顺序
分别表示N2、H2、NH3.观察下图,写出符合在催化剂表面合成氨反应过程的顺序
查看答案和解析>>
科目:初中化学 来源: 题型:
 分别表示N2、H2、NH3.观察下图,写出符合在催化剂表面
分别表示N2、H2、NH3.观察下图,写出符合在催化剂表面
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
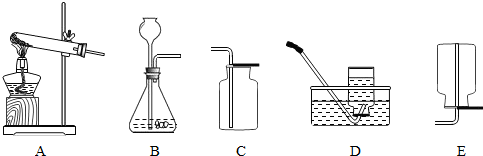
 、
、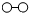 、
、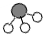 分别表示N2、H2、NH3.在催化剂表面(
分别表示N2、H2、NH3.在催化剂表面( 下图中表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
下图中表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
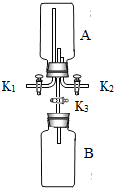 微粒的基本性质”的实验探究,实验过程如下:
微粒的基本性质”的实验探究,实验过程如下:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
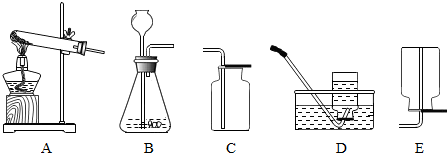
 、
、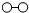 、
、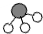 分别表示N2、H2、NH3.在催化剂表面(下图中
分别表示N2、H2、NH3.在催化剂表面(下图中 表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com