
科目:初中化学 来源: 题型:选择题
| A. | 石蕊试液 | B. | Na2CO3溶液 | C. | Fe2(SO4)3溶液 | D. | Cu(NO3)2溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 汽车方便了人们的出行.氢能源汽车备受人们关注
汽车方便了人们的出行.氢能源汽车备受人们关注查看答案和解析>>
科目:初中化学 来源: 题型:填空题
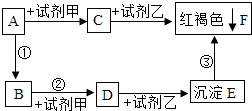 如图所示,A是金属氧化物,B是一种金属单质,C是黄色溶液,D是浅绿色溶液,反应③是物质E与氧气、水发生的一个化合反应,请回答下列问题:
如图所示,A是金属氧化物,B是一种金属单质,C是黄色溶液,D是浅绿色溶液,反应③是物质E与氧气、水发生的一个化合反应,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
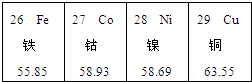
| A. | 镍元素的符号为Ni | |
| B. | 钴元素的相对原子质量是58.93g | |
| C. | 从左到右各元素的原子序数依次增大 | |
| D. | 各元素都属于金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
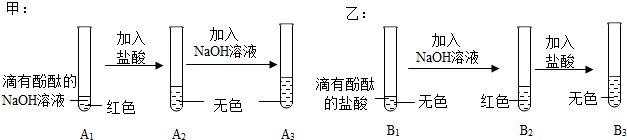
| 探究环节 | 甲同学的探究 | 乙同学的探究 |
| 提出问题 | A3溶液为什么不变红? | B3溶液中溶质成分是什么?(酚酞不计) |
| 做出猜想 | 实验过程中,酚酞变质了? | 猜想一:NaCl 猜想二:NaCl HCl |
| 实验验证 | (1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想不成立(填“成立”或“不成立”) (2)你认为,在常温下A2溶液测出的pH 应<(填“>”、“=”或“<”)7 | 取少量B3溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变浅绿色,据此,你认为乙同学的猜想二(填“一”或“二”)成立 |
| 交流反思 | (1)甲、乙同学的实验中,反应均涉及到的化学方程式是NaOH+HCl=NaCl+H2O. (2)A3溶液未变红,你认为原因是A2溶液中盐酸较多,加入的NaOH溶液未将其完全中和. (3)甲、乙同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制. | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 盐溶液 | NaCl | Na2CO3 | CaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样品溶于水配成溶液,向溶液中滴加CaCl2溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中一定含有Na2CO3(填化学式,下同). |
| ②用玻璃棒蘸取少量①的上层清液滴在pH试纸上,与标准比色卡对照. | pH=11 | 说明久置固体中还一定含有NaOH. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com