
【题目】下列各组物质按单质、氧化物、酸顺序排列的一组是
A. Fe、CO2、H3PO4 B. H2、H2O、NaOH
C. O2、NaOH、H2SO4 D. C、CaO、NaHSO4
科目:初中化学 来源: 题型:
【题目】某化学课外小组的同学,为了测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如右图所示的装置(图中铁架台已经略去),实验在27℃,101kPa下进行。

实验步骤如下:
①按图连接好装置;
②用天平准确称取氢氧化钠样品mg,放入A中试管内,向B中集气瓶内倒入饱和二氧化碳水溶液至瓶颈处;
③向分液漏斗中倒入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞.反应结束后,量筒中收集到饱和二氧化碳水溶液vmL。
④计算氢氧化钠样品中碳酸钠的质量分数。
请回答下列问题:
(1)准确判断氢氧化钠发生变质的实验现象是 ;写出氢氧化钠发生变质的化学方程式 。
(2)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是: 。
(3)B中集气瓶盛装的饱和二氧化碳水溶液不能用水代替,其原因是: 。
(4)判断实验步骤③中滴入的稀硫酸已过量的标志是 。
(5)叙述检验氢氧化钠部分变质的方法:

(6)用上述装置不能准确测定已部分变质的氢氧化钠样品中氢氧化钠的质量分数,理由是 。
(7)取10 g变质的氢氧化钠于烧杯中,其中碳元素的质量分数为6%,向烧杯中加入100 g一定质量分数的稀盐酸(足量),则反应结束后烧杯内物质的总质量是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列问题填空(物质用化学符号表示):
(1) 空气成分中,体积分数为21%的物质是 。
(2) 红磷在空气中燃烧的产物是 。
(3) 能使澄清石灰水变浑浊的气体是 。
(4) 可用于制造硝酸和氮肥的物质是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学取8mL水并加热,提供的仪器有:①10mL量筒;②100mL量筒;③酒精灯;④容积20mL的试管;⑤容积30mL的试管;⑥试管夹,所选用仪器组合正确的一组是
A.②③④⑥ B.①③⑤⑥ C.①③④⑥ D.①②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了验证铁、铜、银的金属活动性顺序,设计了如下实验:
Ⅰ.将铁片浸入稀硫酸
Ⅱ.将铜片浸入稀硫酸
Ⅲ.将铁片浸入硝酸银溶液
(1)上述实验 (选填“能”或“不能”)验证三种金属的活动性顺序。
(2)将铁、铜、银三种金属浸入 溶液(只填一种),即可验证它们的活动性顺序。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高纯硅是制造计算机电路芯片的主要原料。请回答:
(1)硅元素属于 (填“金属”或“非金属”)元素,在地壳中硅元素的含量仅次于_____元素。
(2)硅在氧气中燃烧生成二氧化硅,并放出大量的热,该反应的基本类型为 。
(3)工业上用石英(主要成分为SiO2)制备粗硅的反应为:SiO2+2C![]() Si+2R↑,则R的化学式为 ,反应后硅元素的化合价 (填写“升高”或“降低”)。
Si+2R↑,则R的化学式为 ,反应后硅元素的化合价 (填写“升高”或“降低”)。
(4)生产高纯硅可用三氯硅烷(SiHCl3)。三氯硅烷在空气中极易燃烧,燃烧时可观察到有红色火焰和白色烟,生成物为二氧化硅、氯化氢和氯气,此反应的化学方程式为_____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图为氯化钠、碳酸钠在水中的溶解度曲线。请回答下列问题:

(1)10℃时,碳酸钠的溶解度为 g;
(2)30℃时,氯化钠的溶解度 碳酸钠的溶解度(填写“>”、“<”或“=”);
(3)将碳酸钠不饱和溶液转化为饱和溶液的方法有 、 (至少填两种)。
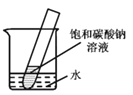
(4)如右图所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是________(填字母序号)。
A.氢氧化钠 B.氯化钠 C.硝酸铵
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组的同学设计了用一氧化碳气体还原氧气铁的实验装置,如图所示,
回答下列问题:
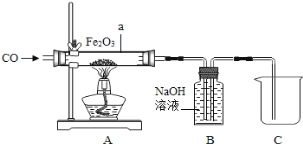
(1)为了避免玻璃管a在加热时可能发生爆炸,加热前应 .
(2)a管中Fe2O3发生反应的化学方程式为 .现象为 。
(3)B装置除了吸收CO2气体外,还 .写出B装置中NaOH发生反应的化学方程式 .
(4)若a管中氧化铁全部还原成铁,冷却后称量铁的质量比反应前氧化铁的质量减少了2.4g,则加入a管中的氧化铁的质量是 g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com