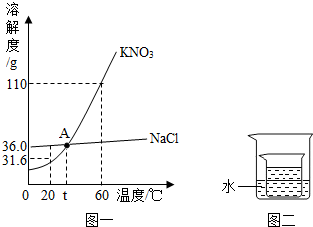
21、2008年初,我国南方地区遭受了一场特大雪灾,道路结冰,给交通带来极大不便.为了快速消除道路上的积雪,交通部门使用了大量的融雪剂,某公司生产的融雪剂是由NaCl、CaCl
2、Na
2CO
3和CuSO
4中的一种或两种物质组成.化学兴趣小组的小红和小兰对融雪剂产生很大的兴趣并对融雪剂的成分进行积极的探究.
[探究实验一]取一定量的融雪剂分装两支试管,进行如下实验,现象记录如下:
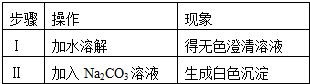
[分析思考]融雪剂中一定含有
CaCl2
,一定不含有
Na2CO3
、
CuSO4
.由此看初步确定其成分有两种可能性:①
NaCl和CaCl2
,②
CaCl2
.
[探究实验二]为了进一步确定该融雪剂的成分,小红、小兰根据不同物质溶于水时的温度变化不同设计了如下实验:将等质量的NaCl固体、融雪剂、CaCl
2固体分别溶于等体积的水中,并用温度计测定溶液的温度,装置如如图所示.
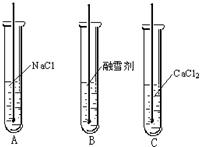
[结论分析]小红、小兰预测:若装置B中温度计的读数介于装置A、C中温度计的读数之间,则可确定融雪剂的成分为
NaCl和CaCl2
.(用化学式表示)
[评价与反思]
①实际操作中,测得A、B、C三个装置中温度计的读数非常接近,没有达到预期的结果.试分析实验失败的原因可能是
取用于实验的三种固体物质的质量不足或没有保温措施等
.(只写一方面的原因即可)
②如果使用大量融雪剂会对周围环境造成的影响是
因融雪剂溶解后会污染水、污染土壤或会加快钢铁桥梁的锈蚀或对公路周围农作物的生长影响等
.(只写一方面的影响即可)

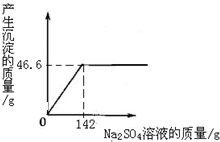
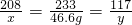
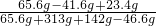 ×100%=10%
×100%=10%



 .
.
 某研究性学习小组设计并进行了如下实验.
某研究性学习小组设计并进行了如下实验.