
科目:初中化学 来源: 题型:阅读理解
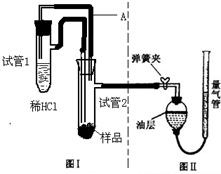 轻质碳酸镁(化学式为4MgCO3?Mg(OH)2?4H2O)是制取氧化镁、颜料、油漆、日用化妆品的工业原料.
轻质碳酸镁(化学式为4MgCO3?Mg(OH)2?4H2O)是制取氧化镁、颜料、油漆、日用化妆品的工业原料.
| ||
查看答案和解析>>
科目:初中化学 来源:2010-2011学年江苏省镇江中学中考化学二模试卷(解析版) 题型:解答题
 4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.
4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.
查看答案和解析>>
科目:初中化学 来源:2011年江苏省扬州市九年级网上阅卷适应性测试化学试卷(解析版) 题型:解答题
 4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.
4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.
查看答案和解析>>
科目:初中化学 来源:2011年江苏省南通市如东县中考化学能力测试试卷(解析版) 题型:解答题
 4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.
4MgCO3?Mg(OH)2?4H2O+CO2↑+10H2O.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com