
【题目】下列装置可制取有关气体。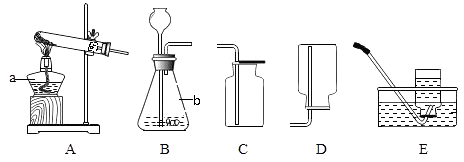
请回答:
(1)仪器a、b 的名称是:a ;b ;
(2)实验室用高锰酸钾制取氧气的化学方程式为;如用E 装置收集氧气,当观察到时,再把导管口伸入盛满水的集气瓶中。
(3)实验室制取二氧化碳的化学方程式为 , 应选用的收集装置是。
(4)实验室也可以用A 装置制取二氧化碳(试管口无需棉花),推测其反应物是。
A.NaHCO3 固体
B.大理石与稀盐酸
C.木炭与氧气
(5)下图装置可用来测量生成的O2 的体积,检验该装置气密性的方法是:当把针筒里的活塞内推时,若看到 , 说明气密性良好。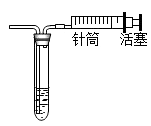
【答案】
(1)酒精灯,锥形瓶
(2)2KMnO4 ![]() K2MnO4 +MnO2 + O2↑,水中的导管口有连续均匀的气泡冒出时
K2MnO4 +MnO2 + O2↑,水中的导管口有连续均匀的气泡冒出时
(3)![]() ,C
,C
(4)A
(5)试管内,导管下端有一段水柱
【解析】(2)加热高锰酸钾分解制取氧气的同时,还生成了锰酸钾和二氧化锰,故反应的化学方程式是2KMnO4 ![]() K2MnO4 +MnO2 + O2↑;E 装置是用排水法收集氧气,由于开始排出来的是空气,故要等气泡连续且均匀冒出时开始收集;(3)实验室用石灰石和稀元素制取二氧化碳,同时还生成了氯化钙和水:
K2MnO4 +MnO2 + O2↑;E 装置是用排水法收集氧气,由于开始排出来的是空气,故要等气泡连续且均匀冒出时开始收集;(3)实验室用石灰石和稀元素制取二氧化碳,同时还生成了氯化钙和水: ![]() ;二氧化碳的密度比空气大,易溶于水,只能用向上排空气法收集,选C装置;(4)A装置属固固加热型,故选A;(5)当把针筒里的活塞内推时,若装置的气密性良好,那么试管中的压强变大,那么导管中的水面会上升。
;二氧化碳的密度比空气大,易溶于水,只能用向上排空气法收集,选C装置;(4)A装置属固固加热型,故选A;(5)当把针筒里的活塞内推时,若装置的气密性良好,那么试管中的压强变大,那么导管中的水面会上升。
【考点精析】利用制取氧气的操作步骤和注意点和书写化学方程式、文字表达式、电离方程式对题目进行判断即可得到答案,需要熟知制取氧气的操作步骤(以高锰酸钾制取氧气并用排水法收集为例)a、步骤:查—装—定—点—收—移—熄;注意:a、配平 b、条件 c、箭号.


科目:初中化学 来源: 题型:
【题目】按照加水溶解、过滤、蒸发的顺序进行操作,可以分离的一组混合物是 。
A.木炭粉和MnO2
B.Fe粉和CuO
C.KMnO4和K2MnO4
D.MnO2和NaCl
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)M元素的单质可用于原子反应堆的导热剂,其原子结构示意图如下:
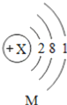
① 该原子有______个电子层,X的值是_______,M元素属于_________(填“金属”或“非金属”)元素;
② M元素的化学性质与下列____________(填序号)元素的化学性质相似。

③ M元素和第②小题的D元素形成化合物的化学式是____________。
(2)世界上的物质都是由粒子构成的,仿照示例填空:
物质名称 | 示例:水 | 铁 | _____ | 氯化钠 |
构成物质的粒子 | 分子 | ____ | 分子 | ______ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近几年我国不少水域多次发生严重的“赤潮”、“水华”现象。“赤潮”、“水华”主要是指水中某些植物营养元素含量过高、导致水面上的藻类疯狂生长、繁殖,水质恶化,造成鱼类死亡。
(1)已知藻类的化学式为C106H263O110N16P,则组成藻类的元素有 , 藻类的相对分子质量为 , 该藻类中氮元素的质量分数是。
(2)根据藻类的化学式确定,工业和生活污水中导致藻类生长过快的营养元素是。
(3)为了解决水体污染,应从控制污染源头着手。下列措施能防止“赤潮”、“水华”现象发生的是(填序号)。
①在水域沿岸新建的住宅小区、饭店、宾馆采用生活污水净化装置;
②两岸居民禁止使用含磷酸钠的洗衣粉;
③禁止用该水域的水进行农业灌溉;
④向该水域中加入大量的净水剂和消毒剂。
(4)“水华”现象一般发生在枯水期还是汛期?为什么?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组利用下图装置对二氧化碳的性质进行探究,下列说法错误的是
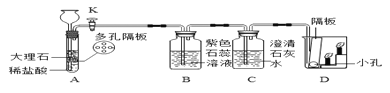
A. B处现象说明二氧化碳能使紫色石蕊变红
B. C处溶液变浑浊,是因为生成了不溶于水的碳酸钙
C. D处的实验现象是下层蜡烛先熄灭,上层蜡烛后熄灭
D. D处现象说明二氧化碳不可燃,不助燃,密度比空气大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】动自行车、小汽车等交通工具中都有为其提供电能的铅蓄电池(又称“电瓶”),它的优点是可以充电循环使用。电瓶的正极材料是二氧化铅(PbO2),负极材料是金属铅(Pb),电瓶内所加液体是溶质质量分数为36%的稀硫酸,放电(为外界供电)时发生反应的化学方程式如下:PbO2(固)+2H2SO4+Pb=2PbSO4(固)+2H2O。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
(1)电瓶在放电时,能转化为电能。
(2)假如某个电瓶中铅的质量为1800 g,内装36%的稀硫酸1200 g,当有310.5 g的铅参加反应时,需消耗稀硫酸中溶质克?此时电瓶中硫酸溶液溶质的质量分数是?(最后结果精确到0. 01%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com