如图1是金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.
(1)选择编号填空:铝的利用比铜和铁晚得多,原因是______;目前铝在多个领域替代易生锈的铜铁,其主要原因是______.
①铝的硬度小 ②铝很活泼 ③地壳中铝的含量高 ④铝的表面易生成致密的保护膜
(2)钢铁的冶炼是人类文明的一个重要标志.如图2是实验室模拟炼铁的装置图,写出冶炼生铁的化学方程式:______ 2Fe+3CO2
【答案】
分析:(1)根据图示可发现,人类大规模开发、利用金属的先后顺序与金属活动必由强到弱的顺序正相反.据此猜测:金属越活泼越难以开发、利用;根据金属铝的性质,对比铝在防止锈蚀的优点;
(2)炼铁的原理是用一氧化碳在高温条件下还原氧化铁.铁能被磁铁吸引.
(3)可燃性气体与空气混合都有可能发生爆炸,所以应先排净空气.
(4)一氧化碳有毒不能直接排放到空气中.
解答:解:(1)在金属活动性顺序中,铝>铁>铜,金属越活泼,越不易冶炼出来,故铝的利用比铜和铁晚得多,铝虽然活动性比铁强,但是表面有致密的氧化物薄膜而导致不易生锈.
故答案为:②;④.
(2)一氧化碳在高温条件下把铁从赤铁矿里还原出来的化学方程式 3CO+Fe
2O
3 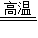
2Fe+3CO
2 ;.生成的铁可被磁铁吸引,或能与酸反应.
故答案为:Fe
2O
3+3CO
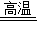
2Fe+3CO
2;用磁铁吸引(或取少量滴入盐酸),观察是否有气泡产生.
(3)可燃性气体与空气混合加热时都有可能发生爆炸,所以应预先把装置内的空气排净.
故答案为:B;排净装置内的空气,以防爆炸.
(4)反应后剩余的一氧化碳排放到空气中会污染空气,所以应对其进行处理,可结合一氧化碳的可燃性进行处理.
故答案为:用点燃的酒精灯烧掉有毒的尾气(或用气球收集).
点评:本题考查了金属活动性顺序的应用以及炼铁的原理,完成此题可以依据课本已有的知识,所以要求同学们在平时的学习中加强基础知识的储备.

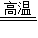 2Fe+3CO2 ;.生成的铁可被磁铁吸引,或能与酸反应.
2Fe+3CO2 ;.生成的铁可被磁铁吸引,或能与酸反应.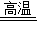 2Fe+3CO2;用磁铁吸引(或取少量滴入盐酸),观察是否有气泡产生.
2Fe+3CO2;用磁铁吸引(或取少量滴入盐酸),观察是否有气泡产生.




