
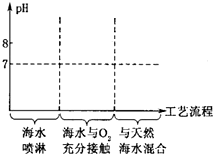
 为了减轻酸雨的危害,我国研发了“海水法烟气脱硫工艺”.其工艺流程大致是:
为了减轻酸雨的危害,我国研发了“海水法烟气脱硫工艺”.其工艺流程大致是:分析 (1)根据海水的pH=8.1-8.3,SO2+H2O=H2SO3H2SO3是弱酸,海水变为弱酸性,pH值逐渐减小,将洗过烟气后的海水与氧气充分接触,发生下列反应:4NaC1+O2十2H2SO3═2Na2SO4+4HC1,盐酸属于强酸,pH值减小到最小,再将与氧气充分接触的海水跟大量天然海水混合等措施,使各项指标接近天然海水后再排放,pH值再次接近pH=8.1-8.3进行分析;
(2)根据硝酸钡和硫酸钠反应会生成硫酸钡沉淀和硝酸钠,然后结合题中的数据进行解答;
(3)根据氯离子和银离子会生成氯化银沉淀进行分析.
解答 解:(1)海水的pH=8.1-8.3,SO2+H2O=H2SO3H2SO3是弱酸,海水变为弱酸性,pH值逐渐减小,将洗过烟气后的海水与氧气充分接触,发生下列反应:4NaC1+O2十2H2SO3═2Na2SO4+4HC1,盐酸属于强酸,pH值减小到最小,再将与氧气充分接触的海水跟大量天然海水混合等措施,使各项指标接近天然海水后再排放,pH值再次接近pH=8.1-8.3,所以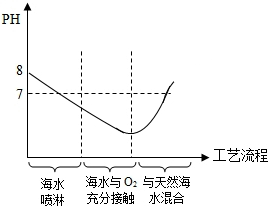
(2)海水样品中Na2SO4含量为x,
Na2SO4+Ba(NO3)2=BaSO4↓+2NaNO3
142 233
x 0.466g
$\frac{142}{x}$$\frac{233}{0.466g}$
x=0.284g;
(3)氯离子和银离子会生成氯化银沉淀,所以要测定海水中NaCl含量,取少量被测海水样品10克,加入足量的硝酸银溶液进行类似实验.
故答案为:(1)
(2)0.284g;
(3)硝酸银.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中所给的提示进行解答.


 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
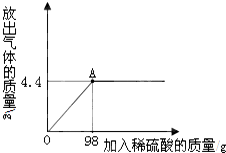 某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀硫酸,测得反应放出气体的总质量与所加入稀硫酸的质量关系曲线如图所示,请根据题意解答问题:
某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀硫酸,测得反应放出气体的总质量与所加入稀硫酸的质量关系曲线如图所示,请根据题意解答问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
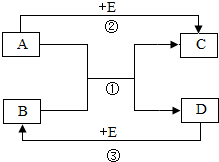 A~E均是初中化学常见的物质,它们的相互转化关系如图所示(反应条件、部分反应物和生成物已略去)
A~E均是初中化学常见的物质,它们的相互转化关系如图所示(反应条件、部分反应物和生成物已略去)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com