
| A. | 向瓶内倒入澄清石灰水振荡 | B. | 在瓶口闻其气味 | ||
| C. | 将带火星的木条插入瓶里 | D. | 将燃着的木条放在瓶口 |
科目:初中化学 来源: 题型:选择题
| A. | 13.3% | B. | 12.3% | C. | 11.3% | D. | 14.3% |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫酸铜溶液和氟化钡溶液 | B. | 氢氧化钙钡溶液和稀硝酸 | ||
| C. | 硫酸和硝酸钾溶液 | D. | 碳酸钾溶液和稀硝酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
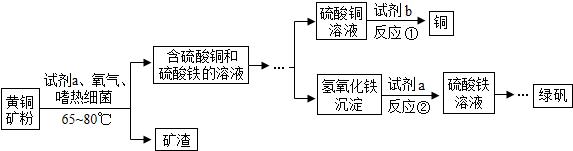
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验编号 | 温度 | 催化剂 | 质量分数 | |
| 甲组实验Ⅰ | 25℃ | 二氧化锰 | 10mL 2%H2O2 | |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
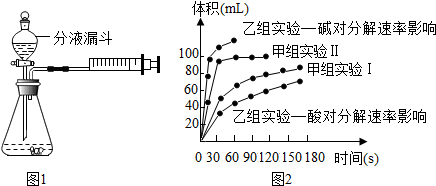
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
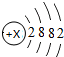 探究元素周期表可寻得一些规律.如图是一些元素的原子结构示意图.例:碳原子结构示意图的意思:6C表示6号元素碳,
探究元素周期表可寻得一些规律.如图是一些元素的原子结构示意图.例:碳原子结构示意图的意思:6C表示6号元素碳,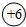 表示核内带6个单位正电荷,
表示核内带6个单位正电荷,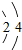 表示核外有6个电子,分两层排布,通常最外层电子数为8时较稳定.
表示核外有6个电子,分两层排布,通常最外层电子数为8时较稳定.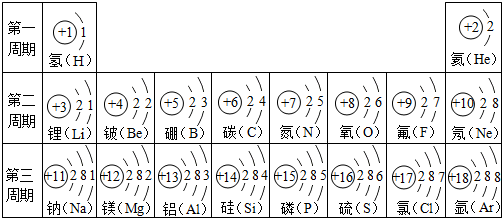
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com