
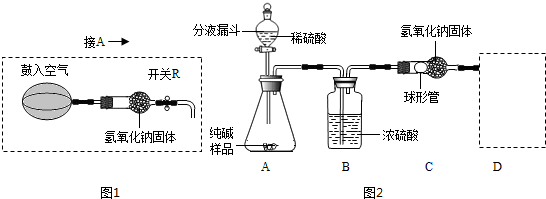
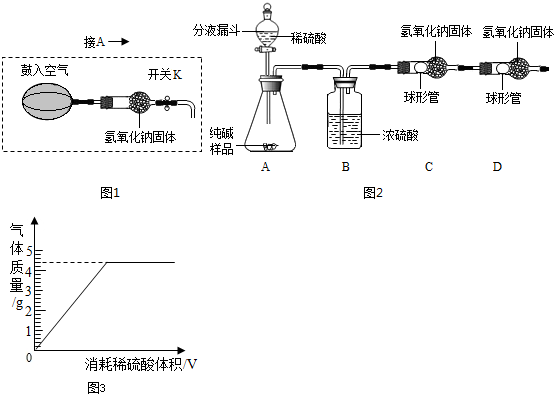
ijƷ�ƴ����к��������Ȼ��ơ�ij��ѧ̽��С��Ϊ�˲ⶨ��Ʒ�ƴ���Ĵ��ȣ���̼���Ƶ�����������������һͬѧ�����ͼ��ʾʵ�飺 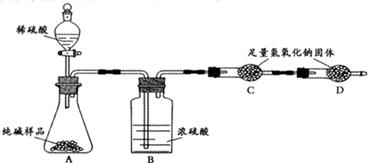
(1)Aװ���з�Ӧ�Ļ�ѧ����ʽΪ ��
(2)Bװ�õ������� ��Cװ���з�Ӧ�Ļ�ѧ����ʽΪ ��
(3) Dװ�õ������� ��
(4)С������ܷ�������������ͬѧ�Ǿ���������Ϊ���ܣ������� ��
(5)С�������Ҫʹ�ⶨ�����ȷ��Ӧ��Aװ�øij�ͼ15��ʾװ�ã����ڷ�Ӧǰ�����������Ŀ����_____________________;��Ӧ��Ҫ�����������Ŀ����_____________________.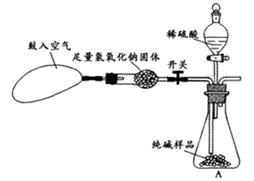
(6)�Ƶô�����Ʒ������Ϊ12.0 g��ʵ��ǰ����Cװ�ã�����ҩƷ���������ֱ�Ϊ61.2 g��65.6 g����ô�����Ʒ�Ĵ���Ϊ %����ȷ��0.1%����
��1��Na2CO3+H2SO4��Na2SO4+H2O+CO2��
��2����ȥˮ���� 2NaOH + CO2 = Na2CO3+ H2O
��3����ֹ�����ж�����̼��ˮ��������Cװ��
(4)����ӷ����Ȼ������屻װ��C���գ�Ӱ��ʵ��ⶨ
(5)�ų�װ���ж�����̼ ʹ���ɵĶ�����̼ȫ������Cװ��
(6) 88.3
�������������(1)Aװ����Ϊϡ�����̼���Ƶķ�Ӧ�����������ơ�ˮ�Ͷ�����̼����2��Cװ����ʢ����Ũ���ᣬĿ��������ˮ������Cװ�����������Ƶ����������ն�����̼��(3)Dװ�õ����������Ƶ����������տ����е�ˮ�����Ͷ�����̼����ֹ����װ�������(4)������ϡ���ᣬ����ӷ����Ȼ������屻װ��C���գ�Ӱ��ʵ��ⶨ��(5)Aװ�õ�ȱ���Dz����Ķ�����̼����һ���ֲ�����Aװ���У����Է�Ӧǰ���������Ϊ���ų�װ���ж�����̼����Ӧ����������Ϊ��ʹ���ɵĶ�����̼ȫ������Cװ�ã�
(6)�贿����Ʒ��̼���Ƶ�����Ϊ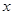 ��
��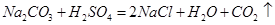
106 44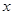 65.6g-61.2g
65.6g-61.2g �����
�����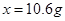
��ô�����Ʒ�Ĵ���Ϊ88.3%.
���㣺̽������ijɷ�
����������һ���dz����͵�̽���⣬��Ŀ����֪ʶ��û��ѧ������Ϊİ���������ص㿼��ķ�Ӧ��˼�룬װ�õȣ�����������Ŀ��Ҫ���£���ϸ���⼴�ɡ�


 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
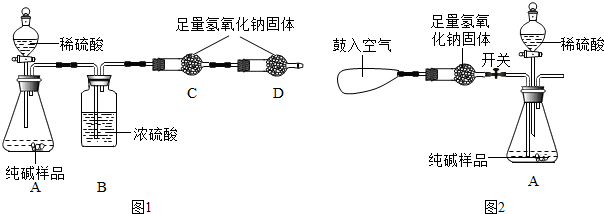
 ��2013?��������ģ��ijƷ�ƴ����к��������Ȼ��ƣ���ѧ̽��С��Ϊ�˲ⶨ�ô���Ĵ��ȣ���̼���Ƶ�������������������ͼװ�ý���ʵ��ⶨ��
��2013?��������ģ��ijƷ�ƴ����к��������Ȼ��ƣ���ѧ̽��С��Ϊ�˲ⶨ�ô���Ĵ��ȣ���̼���Ƶ�������������������ͼװ�ý���ʵ��ⶨ��| ������Ŀ | ����ʱ�� | ����/g |
| ���� | 11.0 | |
| װ��+ϡ���� | 160.0 | |
| װ��+ϡ����+���� | ��Ӧ��ʼ��20s | 167.0 |
| װ��+ϡ����+���� | ��Ӧ��ʼ��30s | 166.6 |
| װ��+ϡ����+���� | ��Ӧ��ʼ��90s | 166.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
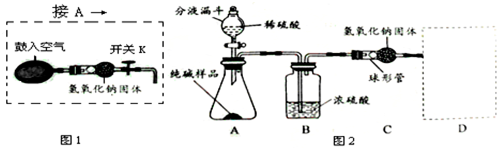
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com