
分析 (1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答;
(2)根据物质中某元素的质量分数=$\frac{该元素相对原子量×原子个数}{该物质的相对分子量}$×100%解决,
(3)依据物质的质量=$\frac{元素的质量}{元素的质量分数}$解决;
解答 解:
(1)相对分子的质量为组成分子的各原子的相对原子质量之和,则有葡萄糖酸亚铁的相对分子质量为12×12+22+56+16×14=446
(2)葡萄糖酸亚铁中铁元素的质量分数=$\frac{56}{446}$×100%=12.6%
(3)若某病人要补充2.8g铁元素,医生开给病人葡萄糖酸亚铁$\frac{2.8g}{\frac{56}{446}×100%}$=22.3g
故答案为:446;12.6%;22.3.
点评 本题主要考查学生对物质中某元素的质量分数知识的理解与掌握,并能在解题中灵活应用的能力.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:计算题
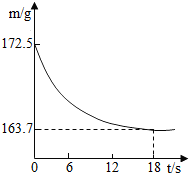 某公司生产出的纯碱产品中经检测只含有氯化钠杂质.在20℃时,称取26.5g该产品加入到盛有一定质量稀盐酸的烧杯中,恰好完全反应,气体完全逸出,得到不饱和NaCl溶液.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示.求:
某公司生产出的纯碱产品中经检测只含有氯化钠杂质.在20℃时,称取26.5g该产品加入到盛有一定质量稀盐酸的烧杯中,恰好完全反应,气体完全逸出,得到不饱和NaCl溶液.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示.求:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图所示,大试管中是螺旋状光亮的铁丝,把试管倒插到水中放置一段时间,观察到铁丝表面有生成,试管内水面将上升,产生现象的原因是铁与氧气、水等物质反应使试管内压强减小.
如图所示,大试管中是螺旋状光亮的铁丝,把试管倒插到水中放置一段时间,观察到铁丝表面有生成,试管内水面将上升,产生现象的原因是铁与氧气、水等物质反应使试管内压强减小.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
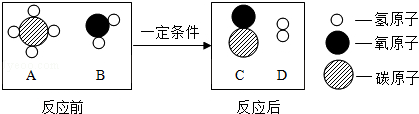
| A. | 该反应中原子个数变少 | B. | 反应前后分子个数不变 | ||
| C. | 反应前后各元素的化合价均不变 | D. | 反应过程中A与D的质量比为8:3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 12 | B. | 16 | C. | 6 | D. | 无法计算 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | S2-:一个硫离子带2 个单位负电荷 | |
| B. | Mn2+:锰元素的化合价为+2 价 | |
| C. | NH3:该物质中N、H 元素的个数比为1:3 | |
| D. | O2:2 个氧原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com