解:(1)生活中经常使用的燃料有煤、石油和天然气等化石燃料;
(2)化石燃料大量使用产生SO
2、NO
2等污染物,这些污染物与形成酸雨有关,会破坏环境;
(3)增大接触面积,和氧气接触充分,有利于物质的燃烧,“蜂窝煤”被加工成多孔形状的原因是增大与氧气接触面积,氧化钙是碱性氧化物,和酸性二氧化硫反应,能减少气体污染;
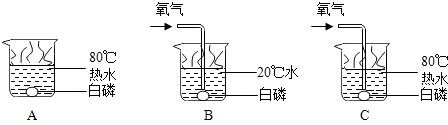
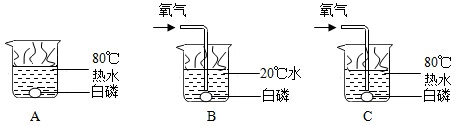
(4)①C中,白磷与氧气接触,温度达到了白磷的着火点,白磷能够燃烧;白磷燃烧的化学方程式为:4P+5O
2
2P
2O
5.
②对比实验B和C可以得到的结论是在与氧气接触的情况下,可燃物必须达到着火点才能燃烧.
故答案为:
(1)石油;
(2)SO
2(写名称给分),酸雨;
(3)增大与氧气接触面积,吸收SO
2,减少空气污染;
(4)①C,4P+5O
2
2P
2O
5,(写加热、不写条件不给分,下同);②可燃物必须达到着火点才能燃烧(围绕控制着火点的意思说的都给分,单说控制温度不给分).
分析:(1)煤、石油、天然气属于化石燃料;
(2)二氧化硫、二氧化氮是形成酸雨的重要物质;
(3)根据有利于物质燃烧的因素并结合氧化钙的性质来回答
(4)根据可燃物燃烧的条件分析,可燃物燃烧的条件分析是:与氧气接触,温度达到着火点.
点评:本题主要考查燃烧的条件和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

 CaSO3,②2CaSO3+O2
CaSO3,②2CaSO3+O2 2CaSO4,
2CaSO4, 2SO3,④SO3+CaO
2SO3,④SO3+CaO  CaSO4.
CaSO4.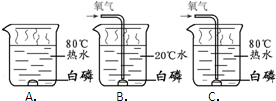
 2P2O5.
2P2O5. 2P2O5,(写加热、不写条件不给分,下同);②可燃物必须达到着火点才能燃烧(围绕控制着火点的意思说的都给分,单说控制温度不给分).
2P2O5,(写加热、不写条件不给分,下同);②可燃物必须达到着火点才能燃烧(围绕控制着火点的意思说的都给分,单说控制温度不给分).

 能源、环境问题是全球关注的热点问题.
能源、环境问题是全球关注的热点问题.
 能源、环境问题是全球关注的热点问题.
能源、环境问题是全球关注的热点问题.