


科目:初中化学 来源: 题型:
 (2012?湘潭)我国铁路将进入“高铁”时代.为将短轨连成长轨,常用下列反应进行焊接:8Al+3X
(2012?湘潭)我国铁路将进入“高铁”时代.为将短轨连成长轨,常用下列反应进行焊接:8Al+3X
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
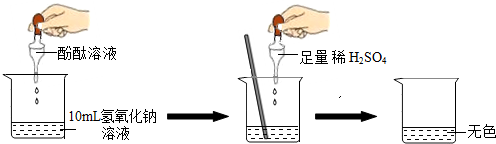
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的BaCl2溶液 | 出现白色沉淀 | 稀H2SO4过量 |
| 方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀H2SO4过量 |
| 方案三 | 取样,加入Na2CO3粉末 | 有气体产生 | 稀H2SO4过量 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com