
如图是氯化钠和硫酸钠的溶解度曲线,看图后回答问题:
(1) 的溶解度收温度影响变化不大.
(2)温度不变时,若将氯化钠的不饱和溶液变为饱和溶液可采取的方法是 .(填一种即可)
(3)40℃时,将30g硫酸钠固体加入到50g水中充分溶解,所得溶液的质量是 g.
(4)用降温结晶的方法提纯含少量杂质氯化钠的硫 酸钠,最佳的温度范围是 ℃以下
酸钠,最佳的温度范围是 ℃以下 ,理由是 .
,理由是 .
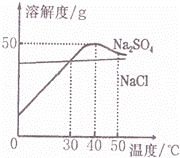
解:(1)据图可以看出,NaCl(或氯化钠)的溶解度收温度影响变化不大,故填:NaCl(或氯化钠).
(2)温度不变时,可以采用加氯化钠(或加NaCl或加溶质或蒸发水分或蒸发溶剂)将氯化钠的不饱和溶液变为饱和溶液,故填:加氯化钠(或加NaCl或加溶质或蒸发水分或蒸发溶剂).
(3)40℃时,硫酸钠的溶解度为50g,将30g硫酸钠固体加入到50g水中充分溶解,只能溶解25g,所得溶液的质量是25g+50g=75g,故填:75.
(4)用降温结晶的方法提纯含少量杂质氯化钠的硫酸钠,需要析出硫酸钠的晶体,从图中可以看出,当温度高于30℃时硫酸钠的溶解度大于氯化钠,低于30℃时硫酸钠的溶解度比氯化钠小,且硫酸钠的溶解大变化比氯化钠明显,故最佳的温度范围是30℃以下,故填:①30℃以下硫酸钠的溶解度比氯化钠小.②30℃以下硫酸钠的溶解度受温度影响变化比氯化钠大.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
生石灰常用作食品干燥剂.久置的生石灰里可能会含有氧化钙、氢氧化钙、碳酸钙三种物质中的一种或几种(假设久制的生石灰中不再含有其它成分).为了探究久置的生石灰的成分,某校化学兴趣小组进行了以下探究活动.
【设计实验】取0.94g久置的生石灰样品放入烧杯中,进行了以下探究实验,如图所示:

【讨论与分析】
(1)生石灰可以做干燥剂的原因是 (用化学方程式表示).
(2)向0.2g滤渣A中滴加稀盐酸,有气泡产生,说明久置的生石灰样品中一定含有 (填写化学式).
(3)②中反应过程中的实验现象是 .
(4)将混合物C、D全部倒入一个洁净的烧杯中混合,充分反应后,过滤,得到1g滤渣E和红色滤液F.向滤液F中滴加CaCl2溶液,有白色沉淀生成,则滤液F的溶质中一定含有 ,还可能含有 .
【解释与结论】依据实验现象和测得的数据判断,0.94g久置的生石灰样品的成分是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
要除去下列各组物质中的少量杂质,所选试剂和方法不可行的是
| 选项 | 物质 | 杂质 | 试剂、方法 |
| A | O2 | 水蒸气 | 通过浓H2SO4洗气 |
| B | MnO2 | 炭粉 | 在空气中灼烧 |
| C | KCl溶液 | BaCl2 | 加入适量的Na2SO4溶液,过滤 |
| D | FeSO4溶液 | CuSO4 | 加入足量铁屑,充分反应后过滤 |
查看答案和解析>>
科目:初中化学 来源: 题型:
右图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.t1℃时等质量甲、乙两种物质的饱和溶液中溶质质量相等
C.t2℃时等质量的甲、乙两物质的饱和溶液降温至t1℃时,
两溶液中溶质质量分数相等
D.氧气的溶解度随温度变化的规律与图中的甲相似
查看答案和解析>>
科目:初中化学 来源: 题型:
推理是化学学习中常用的思维方法.下列推理正确的是( )
|
| A. | 酸和碱能发生中和反应,则硝酸与氢氧化钠也能发生中和反应 |
|
| B. | 铝表面的氧化铝薄膜能起到保护作用,则铁表面的氧化铁也能起到保护作用 |
|
| C. | 碱溶液能使石蕊试液变蓝,则能使石蕊试液变蓝的溶液一定是碱 |
|
| D. | 蔗糖的饱和溶液,不能再溶解蔗糖,也一定不能再溶解其它物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:
央视报道“全国多地相继出现了假干粉灭火器”。干粉灭火器中灭火剂的主要成分是碳酸氢钠,而假干粉灭火器是用面粉做灭火剂。兴趣小组同学想了解学校干粉灭火器中的灭火剂是否报道中的“假干粉”,设计了以下实验进行探究:
探究一:甲、乙两同学分别用物理方法和化学方 法设计方案,进行如下实验:
法设计方案,进行如下实验:

乙同学设计方案中发生的化学方程式为____________________________________。
探究二:小组同学利用该灭火器进行灭火实验后,发现可燃物表面有白色粉末残留。为了解白色粉末的主要成分,继续以下探究:
【查阅资料】1.碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;碳酸钠受热不分解。
2.碳酸氢钠溶解吸收热量;碳酸钠溶解放出热量。
【提出猜想】猜想1:残留物主要成分是碳酸钠; 猜想2:残留物主要成分是__________。
【设计方案】小组同学设计的下列实验方案中,错误的是_____________(填序号)。
A.加热残留物将产生的气体通入澄清石灰水中,若观察到澄清石灰水变浑浊,则猜想2正确
B.将残留物溶于水,若有放热现象,则猜想1正确
C.将残留物溶于水,加过量氯化钙溶液静置,取上层清液加稀盐酸,如产生气泡,则猜想2正确
【反思评价】设计实验方案要思维缜密,考虑周全。用化学知识解释上述错误方案存在的主要问题____________________________ ____________________________________________。
____________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
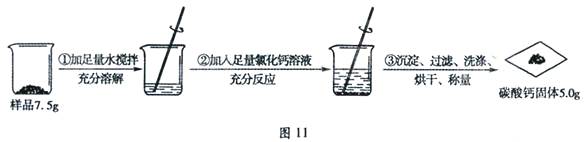
某碳酸钠样品中混有少量氯化钠,根据图11所示信息计算该样品中碳酸钠的质量分数。(计算结果精确到0.1%)
(反应的化学方程式:CaCl2 + Na2CO3 = CaCO3↓+ 2NaCl)
查看答案和解析>>
科目:初中化学 来源: 题型:
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。
(1)请写出镁条与氧气反应的化学方程式_______________。
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律。我_____(“同意”或“不同意”)小明的观点,因为___________。
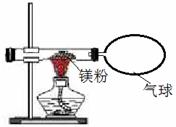 (3)小红按下图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。
(3)小红按下图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象及结论 |
【反思与交流】空气中N2的含量计远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释_____________。
[注意:若答对第(3)小题奖励4分,化学试卷总分不超过60分。]
(4)该兴趣小组又做了镁条与盐溶液反应的实验,发现均能产生H2,实验现象如下:
| 实验序号 | 实验1 | 实验2 | 实验3 | |
| 与镁条反应的溶液 | NH4Cl | NaCl | Na2SO4l | H2O |
| 实验现象 | 有大量气泡产生 | 有较多气泡产生 | 有少量气泡产生 | 气泡极少 |
| 加热后,实验现象 | 气泡明显增多可闻到氨味 | 气泡增多 | 气泡增多 | 气泡增多 |
上表中,用水进行实验的目的是_________________。
根据上表中的实验现象,请写出三条结论,并分析可能的原因(不分析原因,不得分):①__________;②_____________;③______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
下列化学方程式书写正确的是( )
A.Mg+O2===MgO2 B.KClO3===KCl+O3
C.Zn+HCl===ZnCl+H2 D.H2+CuO Cu+H2O
Cu+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com