
分析 (1)根据次氯酸钙分子的构成分析;
(2)化合物中各元素质量比=各原子的相对原子质量×原子个数之比进行分析;
(3)利用组成元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,由次氯酸钙的化学式可计算其中钙元素的质量分数;
(4)根据每50kg饮用水至少需要漂白粉250g的质量关系,判断消毒20kg的一桶水需要漂白粉的质量.
解答 解:(1)一个次氯酸钙分子是由1个钙原子、2个氯原子和2个氧原子构成的,则次氯酸钙中钙、氯、氧三种原子个数比为1:2:2;
故答案为:1:2:2;
(2)钙、氯、氧三种元素的质量比=40:(35.5×2):(16×2)=40:71:32;
故答案为:40:71:32;
(3)次氯酸钙中氯元素的质量分数=$\frac{35.5×2}{40+35.5×2+16×2}$×100%≈49.7%,
故答案为:49.7%;
(4)饮用水每50kg至少需要漂白粉250g,则消毒一桶水(约20kg)至少须加漂白粉=$\frac{20kg}{50kg}×250g$=100g
故答案为:100.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


科目:初中化学 来源: 题型:多选题
| A. | ①②③④ | B. | ④③②① | C. | ④③①② | D. | ③①④② |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
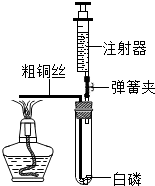 注射器是一种普通的医疗器械,但它在化学实验中发挥着越来越大的作用.某化学兴趣小组为了测定空气中氧气的含量,进行了如下探究活动:
注射器是一种普通的医疗器械,但它在化学实验中发挥着越来越大的作用.某化学兴趣小组为了测定空气中氧气的含量,进行了如下探究活动:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 粗盐久置在空气中会潮解 | |
| B. | 盛有食醋的瓶子打破后,会散发出一种刺激性气味 | |
| C. | 装满水的玻璃瓶结冰后,瓶子炸裂 | |
| D. | 温度和溶剂量不变,久置的食盐水中产生了食盐晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com