
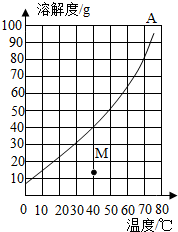
 如图是A物质的溶解度曲线图,如表是B物质在不同温度时的溶解度.
如图是A物质的溶解度曲线图,如表是B物质在不同温度时的溶解度. | 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| B物质溶解度/g | 32 | 35 | 40 | 45 | 55 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)根据表中B物质不同温度下的溶解度利用描点法标出,然后用光滑的曲线连接起来,画出曲线图,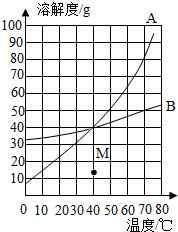
(2)根据A的溶解度曲线和B的溶解度表可看出40℃时两物质的溶解度相等,即饱和溶液中溶质的质量分数相等;
(3)A物质的溶解度受温度影响较大,要想A结晶析出应用降温结晶法,所以小娟同学方法合理;
(4)40℃时,A物质的溶解度是40g,所以将50gA物质加入100g水中,充分溶解后,形成溶液的质量为140g.
故答案为:(1)
(2)40;
(3)小娟;
(4)140.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


 优学名师名题系列答案
优学名师名题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO与CO2化学性质不同,是因为它们的分子构成不同 | |
| B. | NaOH溶液与KOH溶液都能使酚酞溶液变成红色,是因为它们的溶液中都含有OH- | |
| C. | 金刚石和石墨物理性质存在差异,是因为构成它们的碳原子不同 | |
| D. | 温度计受热时,水银柱上升,是因为受热时汞原子间间隔变大 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某化学兴趣小组使用如图所示装置,对某种铁铜合金的成分进行测量,先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品开始计时,并将电子天平的读数记录在表中,请回答下列问题:
某化学兴趣小组使用如图所示装置,对某种铁铜合金的成分进行测量,先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品开始计时,并将电子天平的读数记录在表中,请回答下列问题:| 记录时间 | 空烧杯 | 加入 硫酸后 | 加入铁粉后 5分钟 | 加入铁粉后 12分钟 | 加入铁粉后 21分钟 | 加入铁粉后 40分钟 | 加入铁粉后 3小时 |
| 读数(g) | 28.5 | 169.7 | 183.6 | 183.5 | 183.4 | 183.3 | 183.3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源:2017届江苏省高邮市九年级下学期第一次网上阅卷适应性训练(一模)化学试卷(解析版) 题型:信息分析题
化学用语是学习化学的重要工具。
(1)用化学符号表示:
① 氮元素___________;② 2个铵根离子_________;③ 葡萄糖___________;④ 硫酸根离子___________。
(2)选择下列适当的物质填空(填字母序号):
A.氧气 B.硫酸铜 C.糖类 D.聚乙烯 E.维生素C F.硝酸钾
①用于食品包装_________;②属于复合肥料的是___________;③蔬菜中富含的营养物质___________;
④大米富含_____________;⑤可供呼吸的气体___________;⑥配制波尔多液的盐是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com