
 如图,回答问题:
如图,回答问题:分析 根据酒精灯火焰的分层和外焰温度最高解答.
解答 解:(1)酒精灯灯焰由内向外分焰心、内焰和外焰三个部分;
(2)由于三层火焰的温度不同,如果把火柴梗放入火焰中,它被烧的程度不同,现象也不同,外焰温度最高,从图中可知a处在蜡烛燃烧的外焰,所以a处最先碳化.外焰与氧的接触面积最大,燃烧最充分温度最高,给物质加热需要用酒精灯的外焰.
(3)将一只干冷的烧杯罩在蜡烛火焰上方,烧杯内壁出现水珠,片刻后取下烧杯,迅速向烧杯内倒入少量澄清的石灰水,振荡后发现石灰水变浑浊,可得出蜡烛燃烧生成水和二氧化碳的结论.
故答案为:(1)外焰;内焰;焰心;(2)a;外焰温度最高;(3)水珠;石灰水变浑浊.
点评 了解酒精灯火焰的分层情况,知道如何正确的使用酒精灯.


科目:初中化学 来源: 题型:选择题
| A. | 可观察到蜡烛燃烧产生明亮的火焰,火焰分三层 | |
| B. | 蜡烛熔化产生“烛泪” | |
| C. | 用燃着的火焰去点燃蜡烛刚熄灭时的白烟,蜡烛不能复燃 | |
| D. | 蜡烛燃烧后的产物是二氧化碳和水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
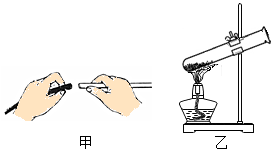 科学实验要注意正确的操作方法,否则会损坏仪器或带来安全威胁.
科学实验要注意正确的操作方法,否则会损坏仪器或带来安全威胁.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据下图的溶解度曲线回答下列问题:
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据下图的溶解度曲线回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加热前试管外壁干燥 | |
| B. | 没有预热,加热不均匀,局部温度过高 | |
| C. | 试管口略向下倾斜了 | |
| D. | 试管夹夹在试管中上部了 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
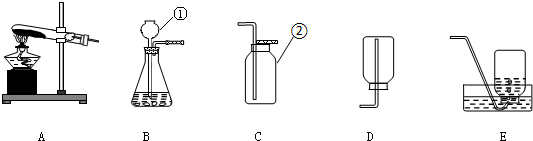
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 收集一集气瓶氢气,将带火星的木条放在集气瓶口验满 | |
| B. | 粗盐提纯过滤盐水时,还要用玻璃棒轻轻搅动漏斗中的液体 | |
| C. | 某溶液中加入用盐酸酸化了的氯化钡溶液有白色沉淀生成,说明有硫酸根 | |
| D. | 检验装置的气密性要在加放试剂之前进行 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入稀硫酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
| 充分反应后剩余固体的质量(g) | 8 | 6 | 4 | 2 | 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com