(2008?随州)马坪中学化学兴趣小组对“双氧水溶液与二氧化锰制氧气“进行了下列实验与探究:
a.在试管中加入5mL 5%的H
2O
2溶液,观察无气泡产生
b.向另一支试管中加入少量MnO
2,然后缓缓加入5mL 5%的H
2O
2溶液,观察、有大量气泡产生
(1)请你用常规方法检验b实验中产生的气体是氧气
将带火星的木条伸入试管中,木条复燃
将带火星的木条伸入试管中,木条复燃
.
(2)按照b的操作制取O
2不宜控制气流速度.为了得到平稳的氧气流,请你设计一个合理操作
在试管中加入少量MnO2,然后通过分液漏斗逐滴滴加5mL5%的H2O2溶液
在试管中加入少量MnO2,然后通过分液漏斗逐滴滴加5mL5%的H2O2溶液
.
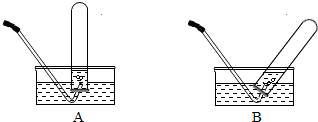
(3)用排水法收集O
2,为了使试管内收集满O
2,你将选择下列
A
A
装置.
(4)该小组还对溶液浓度、温度等实验条件进行了探究.他们对用足量等体积H
20
2溶液制取相同体积O
2所需时间进行了测定,部分数据如下表:
条件
时间(min)
催化剂 |
60℃时,20%H202 |
40℃时,20%H202 |
20℃时,10%H202 |
20℃时,5%H202 |
| 不加催化剂 |
|
|
|
|
| 加等量MnO2 |
0.3 |
0.5 |
1.O |
1.8 |
请你结合他们的实验数据分析:若不加催化剂,60℃水浴条件下,用常规方法检验盛有20%H
20
2溶液的试管中产生的0
2,结果现象不明显,其可能原因是
产生氧气量不足
产生氧气量不足
;你从上表数据分析还可以得到哪些结论?
温度越高反应越快,浓度越大反应越快
温度越高反应越快,浓度越大反应越快
.

 (2008?随州)马坪中学化学兴趣小组对“双氧水溶液与二氧化锰制氧气“进行了下列实验与探究:
(2008?随州)马坪中学化学兴趣小组对“双氧水溶液与二氧化锰制氧气“进行了下列实验与探究:
