
【题目】阅读下面科普短文
多孔活性炭具有较好的吸附性能,是一种优良的催化剂载体材料,广泛应用于各行各业,其生产一直以煤、竹子、木材等宝贵资源为原料。随着可持续发展理念的不断深入,越来越多的研究者尝试以清洁廉价的资源作为原料(如白酒糟),制备多孔活性炭。
白酒糟是酿酒过程的副产物,富含纤维素[(C6H10O5)n]。以白酒糟为原料生产多孔活性炭的过程主要包括干燥、炭化、活化三步。炭化过程是将干燥的白酒糟在充满氮气的环境中,加热至650 ℃,将其中的纤维素转化为炭质原料(主要成分为单质碳)。活化过程是以水蒸气或CO2为活化剂,在一定条件下使其在炭质原料内部发生反应,生成气体,形成孔隙结构,制备多孔活性炭。以CO2为活化剂时,发生的化学反应如下: C + CO2 =2CO,也有研究者在其他条件相同的情况下,通过实验测定所得多孔活性炭对碘的吸附值与水蒸气、CO2用量的关系分别如图1、2所示。
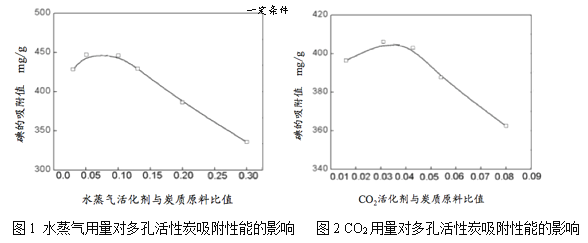
尽管以白酒糟为原料,制备多孔活性炭材料的技术仍有许多问题有待于进一步探索、解决,但已有研究为富含纤维素工业残渣的利用提供了可能途径。
依据文章内容,回答下列问题。
(1)以白酒糟为原料制备多孔活性炭的优点是_____。
(2)炭化过程中,需将干燥的白酒糟置于氮气环境中,理由是_____。
(3)水蒸气与炭质原料在高温条件下发生置换反应,可生成一氧化碳。该反应的化学方程式为_____。
(4)下列说法正确的是_____(填字母序号)。
A 白酒糟富含纤维素
B 多孔活性炭可用于净水
C 水蒸气用量越多,制得的多孔活性炭的吸附性能越好
(5)由图1、图2数据可知,为了达到最佳吸附效果,应选用的活化剂是_____(填“水蒸气”或 “CO2”)。
【答案】白酒糟是清洁廉价的资源 防止碳(或纤维素/白酒糟)与氧气(或空气)反应 C+H2O![]() CO+H2 AB 水蒸气
CO+H2 AB 水蒸气
【解析】
(1)根据“越来越多的研究者尝试以清洁廉价的资源作为原料(如白酒糟),制备多孔活性炭”可知,白酒糟是清洁廉价的资源,用来制备多孔活性炭时,能够实现变废为宝;
(2)氧气是一种化学性质较活泼的气体,能与许多物质反应。炭化过程中,需将干燥的白酒糟置于氮气环境中,理由是防止碳(或纤维素/白酒糟)与氧气(或空气)反应;
(3)水蒸气与炭质原料在高温条件下发生置换反应,可生成一氧化碳,该反应的化学方程式为:C+H2O![]() CO+H2;
CO+H2;
(4)A 根据题中信息“白酒糟是酿酒过程的副产物,富含纤维素[(C6H10O5)n]”可知,白酒糟富含纤维素,故A正确;
B 多孔活性炭具有吸附性,可用于净水,故B正确;
C 由图1可知,不是水蒸气用量越多,制得的多孔活性炭的吸附性能越好,故C错误。故选AB;
(5)由图1、图2数据可知,为了达到最佳吸附效果,应选用的活化剂是水蒸气,这是因为水蒸气作活化剂时,对碘的吸附值最高能够达到440mg/g,而二氧化碳作活化剂时,对碘的吸附值最高能够达到404mg/g。


科目:初中化学 来源: 题型:
【题目】中国古代化工厅。该厅主要展示中华民族古代化工对世界文明做出的重要贡献,展示内容有制陶烧瓷、金属冶炼、造纸发明、火药火器等。
(1)陶瓷的主要成分之一是硅酸钙(CaSiO3),其中硅元素的化合价是_______。
(2)铜是人类最早利用的金属之一,下列铜制品利用金属导热性的是_______(填字母)。
A铜火锅 B 铜导线 C铜钱币
(3)东汉时期铜制“马踏飞燕”是金属冶炼与艺术的完美结合,主要材质是利用硫酸铜溶液和铁的反应制备而成,该反应的化学方程式是:_________________。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于2CO+O2![]() 2CO2的理解不正确的是( )
2CO2的理解不正确的是( )
A. 表示一氧化碳与氧气在点燃条件下反应生成二氧化碳
B. 参加反应的一氧化碳与氧气的质量比为5:4
C. 反应前后碳原子、氧原子的个数均不变
D. 参加反应的氧气与生成的二氧化碳的分子个数比为1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了验证锌、铁、铜的金属活动性强弱,同学们设计了如如图所示实验。

(1)实验A的目的是_________。
(2)实验B能证明金属活动性铁强于铜的实验现象是________。
(3)实验C也能验证铁与铜的金属活动性强弱,则X、Y分别是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命的源泉。
①净水器可以净化自来水,净水器中装有活性炭,其作是_______;净水器接通电源时产生紫外线与自来水生产中加氯气的目的相同,其作用_______。
②如图表示电解水的简易装置。请回答下列问题:
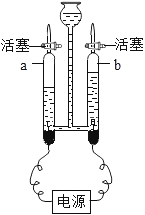
Ⅰ.a试管中产生的气体是_______;检验b试管中气体的方法是_______;a试管和b试管中产生气体的体积比约等于_______;电解水反应的化学方程式为_______,该反应的基本类型是_______。
Ⅱ.如果将电解水产生的氢气直接缓缓地通过装有足量无水硫酸铜的仪器c,在导管口d处点燃,然后把盛有冷水的烧杯置于如图所示的位置。实验过程中可以观察到的现象是_______,C中发生反应的化学方程式是_______。
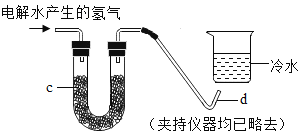
Ⅲ.能证明水是由氧元素和氢元素组成的实验是_______。
a.水的净化 b.水的蒸发 c.水的电解 d.氢气在氧气中燃烧
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】C60可用作吸氢材料,其原理是C60与H2在一定条件下反应生成氢化物;该氢化物在80 ~ 215 ℃时,会分解放出H2。
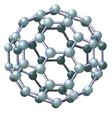
(1)C60属于_____(填字母序号)。
A 单质 B 化合物 C 混合物
(2)求算C60的相对分子质量的计算式为_____。
(3)C60可用作吸氢材料是利用了其_____(填“物理”或“化学”)性质。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧化铝在生产生活中应用广泛。以铝土矿(主要成分是Al2O3)为原料,生产氧化铝的工艺如下
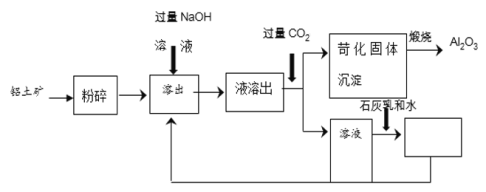
(1)粉碎:用粉碎机将铝土矿石粉碎成粉末。粉碎的目的是________。
(2)溶出:用过量的NaOH溶液将粉碎的铝土矿中难溶性Al2O3转化成可溶性NaAlO2,形成溶出液。溶出时,发生化学反应:2NaOH + Al2O3= 2NaAlO2 + H2O。溶出液中一定含有的溶质是_______。
(3)苛化:向含有Na2CO3的废液中加入石灰乳[Ca(OH)2与水的混合物]。Na2CO3与石灰乳反应的化学方程式为_____。
(4)该生产工艺中,可以循环使用的物质是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组在探究硫酸铜的化学性质时,做了如图所示的三组实验.

(1)实验一:探究硫酸铜溶液的酸碱性,用pH试纸测得pH<7,则说明硫酸铜溶液呈 性.
实验二:探究硫酸铜溶液与金属的反应.观察到试管A中有 现象时,说明铁与硫酸铜溶液发生了反应;而试管B中无明显现象,则铜、铁、银三种金属活动性由强到弱的顺序依次是 .
实验三:探究硫酸铜与碱溶液的反应.观察到试管C中产生蓝色沉淀,该反应的化学方程式为 .
(2)小组同学将实验三中所得混合物过滤,得蓝色固体和无色滤液.对滤液中溶质的成分展开探究.
【提出问题】滤液中溶质的成分是什么?
【猜想假设】滤液中溶质的成分有 种可能.
【实验验证】取少量滤液与试管中,向其中滴加几滴无色酚酞溶液,溶液变红,则滤液中的溶质是 .
【拓展迁移】小组同学欲将得到的蓝色固体转化成硫酸铜溶液,可向其中加入适量的 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在日常生活中有着广泛的用途。常见金属的活动性顺序如图

请回答下面问题:
(1)金属活动性顺序表中的X是_____元素。(填元素符号)
(2)把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,该反应的化学方程式为_____
(3)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间的变化情况如图2所示。图中B点溶液中含有的溶质有_____(填化学式)
(4)为比较三种金属活动性大小,进行如图3实验。三种金属的活动性顺序是_____
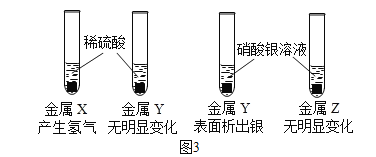
(5)非金属单质也具有类似金属与盐溶液之间发生置换反应的规律,即活动性较强的非金属可把活动性较弱的非金属从其盐酸溶液中置换出来,如在溶液中可发生下列反应:
Cl2+2NaBr=2NaCl+Br2、I2+Na2S=2NaI+S↓、Br2+2KI=2KBr+I2
由此判断S、Cl2、I2、Br2四种单质中非金属活动性最强的是_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com