
【题目】金属及其金属制品对人类社会的发展有着极其重要的作用。
汽车制造过程中要用到大量的铁、铜、铝等金属材料,请按要求填空。
(1)汽车制造中用得最多的金属材料是钢。钢____(填“是”或“不是”)纯金属。为了防止车体表面生锈,车体要进行____。炼铁的原理是利用一氧化碳与氧化铁反应还原出铁,反应的化学方程式为___________________。
(2)汽车电路中的导线大都是铜芯的,这主要是利用了铜的____性。将赤铜矿(主要成分Cu2O)和辉铜矿(主要成分Cu2S)混合焙烧可得到铜,请将反应的方程式补充完整:2Cu2O+Cu2S![]() 6Cu+____。
6Cu+____。
(3)铁、铜、铝三种元素在地壳中的含量最大的是_______,但三种金属被人类发现和利用的时间是铜最早,而铝最晚,主要是因为铝具有很好的抗腐蚀性能,原因是______(用化学方程式表示)。
(4)为了探究铝、铁、银三种金属活动性顺序,可选择Al、Ag和____来进行实验。
【答案】不是 喷漆 3CO+Fe2O3![]() 2Fe+3CO2↑ 导电 SO2↑ 铝(Al) 4Al+3O2=2Al2O3 FeSO4溶液(FeCl2溶液或Fe(NO3)2溶液也可)
2Fe+3CO2↑ 导电 SO2↑ 铝(Al) 4Al+3O2=2Al2O3 FeSO4溶液(FeCl2溶液或Fe(NO3)2溶液也可)
【解析】
(1)钢是由铁和碳组成的合金,所以钢不是纯金属;铁生锈的主要条件是与空气和水直接接触,如果隔绝了空气和水,就能在一定程度上防止钢铁生锈,在钢铁表面涂油、刷漆、镀耐磨和耐腐蚀的铬及制造耐腐蚀的合金如不锈钢等,都能防止钢铁生锈,所以为了防止车体表面生锈,车体要进行喷漆;炼铁的化学方程式为3CO+Fe2O3![]() 2Fe+3CO2↑。
2Fe+3CO2↑。
故填:不是;喷漆;3CO+Fe2O3![]() 2Fe+3CO2↑。
2Fe+3CO2↑。
(2)物质的性质决定用途,铜能用作汽车电路中的导线主要是利用了铜的导电性;根据质量守恒定律,在化学反应前后原子的种类和数目都不变,由方程式可知,反应物中含有的元素种类及原子个数分别为 Cu,6;O,2;S,1;已知生成物中的元素种类及原子个位数分别为 Cu,6;比较可知生成物缺少S元素和O元素,S原子个数为1,O原子个数为2,故化学式为SO2。
故填:导电;SO2↑。
(3)地壳中元素含量由多到少前六个的顺序为氧、硅、铝、铁、钙、钠,故铁、铜、铝三种元素在地壳中的含量最大的是铝;铝具有很好的抗腐蚀性能是因为铝与氧气反应生成致密的氧化铝薄膜对铝起到保护作用,其反应的化学方程式为4Al+3O2=2Al2O3。
故填:铝(Al);4Al+3O2=2Al2O3。
(4)可以通过金属与金属盐溶液之间相互置换的反应来探究或验证金属的活动性顺序,要探究铝、铁、银三种金属活动性顺序,可选择Al、Ag和FeSO4溶液(FeCl2溶液或Fe(NO3)2溶液也可)来进行实验,把铝丢入FeSO4溶液中,溶液由浅绿色变为无色,铝能置换出FeSO4溶液中的铁,金属活动性铝>铁,把银丢入FeSO4溶液中,无明显现象,银不能置换出FeSO4溶液中的铁,金属活动性铁>银。
故填:FeSO4溶液(FeCl2溶液或Fe(NO3)2溶液也可)。


科目:初中化学 来源: 题型:
【题目】同学在实验室里用高锰酸钾制取收集氧气,并进行氧气的性质实验,结合下列实验装置图回答问题:

(1)写出指定仪器的名称:a_____。
(2)请为该同学选择制取氧气的发生装置_____,若选用C装置来收集氧气,如何验满:_____。
(3)若用E装置收集的氧气不纯,其原因可能是_____。某同学用高锰酸钾制取氧气,实验结束后,发现水槽内的水变成了紫红色,可能的原因是_____。如果用F装置收集氧气,气体应从_____(选填“a”或“b”)端管口通入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学活动小组合作学习氢氧化钠和氢氧化钙的相关知识。如表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
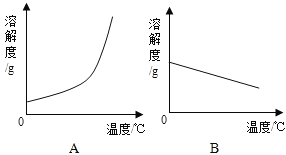
(1)依据上表数据,绘制了Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是_____(填“A”或“B”)。
(2)将一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入适量氢氧化钙②升高温度③降低温度④加入水⑤蒸发水后再恢复到原温度⑥加入适量生石灰。
其中措施在原理上正确的是_____(填字母)
A ②④⑥ B ③④ C ①②⑤⑥ D ①②⑤
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH固体。这时溶液的质量分数为_____
(4)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH_____(填“偏大”或“偏小”“不受影响”)。
(5)可鉴别氢氧化钠溶液和澄清石灰水的一个化学反应方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人类的宝贵自然资源。请分析图回答问题:
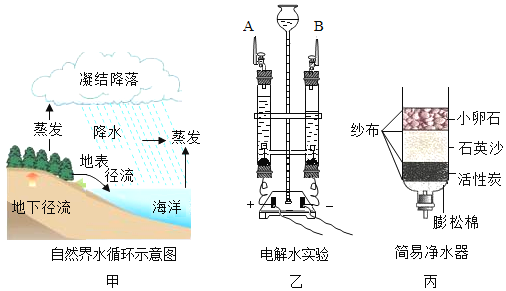
(1)甲图海洋中含有大量氯化钠(俗名食盐),请用适当的符号表示氯化钠的构成微粒:_____。
(2)甲乙两图比较,变化前后水分子本身不变的是_____图。
(3)检验乙图AB两管产生的气体是氢气还是氧气最好用_____检验时B管口处的现象是_____通过电解水实验,证明水是由_____组成的。
(4)图中纱布小卵石、石英砂活性炭和膨松棉的共同作用是_____,除此之外活性炭还起_____作用。
(5)若将河水通过丙图装置处理,所得到的液体是纯净物还是混合物_____?
(6)自来水厂可用+4价氯元素的氧化物消毒,此氧化物的化学式是_____
(7)区别开硬水和软水可用_____。生活中常用的方法_____降低水的硬度,同时又能起消毒作用。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关化学用语中数字“2”的意义的说法,错误的是( )
①3SO2 ②Mg2+ ③CO2 ④![]() SO4 ⑤O2﹣ ⑥H2O2.
SO4 ⑤O2﹣ ⑥H2O2.
A.表示分子个数的是①
B.表示离子所带电荷数的是②⑤
C.表示化合价数值的是④
D.表示一个分子中含有某种原子个数的是①③⑥
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学革命是发生在十八世纪末英国和法国的一场深刻的化学学科的变革。英国物理学家、化学家波义耳和法国化学家拉瓦锡曾做过貌似相同的两个实验(见图)。
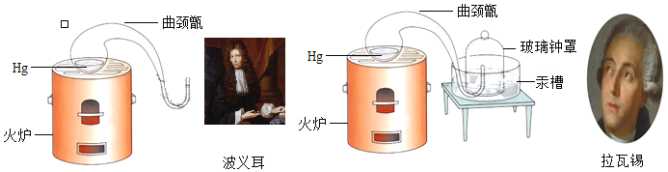
关于这两个实验的说法正确的是( )
A. 两个实验都可用于测定空气中氧气的含量
B. 两个实验中,曲颈甑内汞的表面都变为黑色
C. 波义耳的实验中,金属加热后质量增加,该现象不能用质量守恒定律解释
D. 拉瓦锡的实验中,玻璃钟罩内液面逐渐上升,达到一定高度后不再变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室部分仪器或装置如图所示,请回答下列问题:
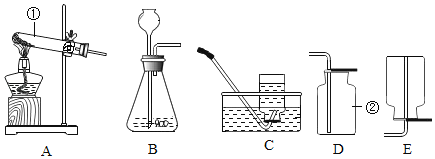
(1)标号①②的仪器名称:①_____②_____
(2)实验室常温下用过氧化氢溶液和二氧化锰的混合物制取氧气,其发生装置和收集装置的组合为_____,反应的文字表达式为_____。
(3)用B装置制取氧气时,反应速率比较快,可能导致实验变得不安全,你准备采用的改进措施是_____
(4)实验室选择AC装置制取氧气,反应的文字表达式为_____,收集完氧气后,应进行的操作是_____。(填①先撤离导管,再熄灭酒精灯或者②先熄灭酒精灯,再撤离导管。)理由是_____,若用C装置收集的氧气不纯,原因可能是_____(写一种即可),验满的方法是_____
(5)用收集到的氧气做细铁丝燃烧的实验:
①铁丝为什么要绕成螺旋状?_____
②集气瓶内为什么要预先装少量水或铺一层细沙?_____
③铁丝在氧气中燃烧的文字表达式_____
(6)已知甲烷是一种无色无味、密度比空气小,难溶于水的气体,实验室常用加热无水醋酸钠与碱石灰的固体混合物来制取甲烷,则实验室制取并收集甲烷选择的装置组合为_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】由以下粒子结构示意图得出的结论错误的是( )
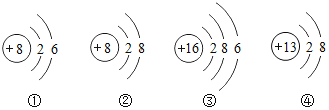
A. ④表示的阳离子
B. ③表示的元素位于元素周期表第六周期
C. ②④形成的化合物是A12O3
D. ①②属于同种元素,①③化学性质相似
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸铵((NH4)2SO4)是一种常用的化肥,它为农作物补充生长所需的氮元素。请根据化学式回答下列问题:
(1)硫酸铵由_____种元素组成,其中氮元素的化合价是_____;
(2)计算硫酸铵的相对分子质量_____(要有必要的过程,下同);
(3)计算硫酸铵中各元素的质量比_____;
(4)计算硫酸铵中氮元素的质量分数_____(保留一位小数);
(5)若今年种植玉米需要补充氮元素42.4千克,约需要硫酸铵多少千克_____?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com