
【题目】随着环境问题的日益严重,垃圾的处理问题正日益被人们所重视。某垃圾处理厂对金属垃圾(主要成分是铁、铜、氧化铁、二氧化硅)的处理及综合利用的部分工艺如图所示。请回答下列问题:
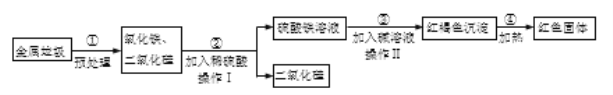
(1)Ⅰ、Ⅱ均为____操作,此操作中玻璃棒的作用是_____,若得到的硫酸铁溶液有浑浊,原因可能是__________。
(2)步骤③所发生的反应属于基本反应类型中的_________________。
(3)请写出步骤②所发生反应的化学方程式:____________________。
(4)写出所得红色固体的一种用途:_____________________________。
【答案】 过滤 引流 滤纸破损 复分解反应 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O 炼铁
【解析】对金属垃圾(主要成分是铁、铜、氧化铁、二氧化硅)的处理及综合利用。稀硫酸与铁、氧化铁反应分别生成硫酸亚铁和硫酸铁,与铜、二氧化硅不反应;硫酸铁溶液与氢氧化钠溶液反应生成氢氧化铁红褐色沉淀;氢氧化铁加热生成氧化铁红色固体。(1)Ⅰ、Ⅱ均为过滤,过滤是把不溶于液体的固体物质与液体分离的一种方法;此操作中玻璃棒的作用是引流,若得到的硫酸铁溶液有浑浊,原因可能是滤纸破损或滤液超出滤纸边缘。(2)步骤③所发生的反应属于基本反应类型中的复分解反应,硫酸铁与氢氧化钠均属于化合物,反应后生成氢氧化铁和硫酸钠也均属于化合物。(3)步骤②所发生反应的化学方程式:Fe2O3+3H2SO4 =Fe2(SO4)3+3H2O。 (4)红色固体的一种用途:氧化铁可以炼铁。
点睛∶氢氧化铁是红褐色沉淀,氧化铁是红色固体。稀硫酸与铁、氧化铁反应;与铜、二氧化硅不反应。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】以下是初中化学的一些基本实验,请根据实验内容回答下列问题。
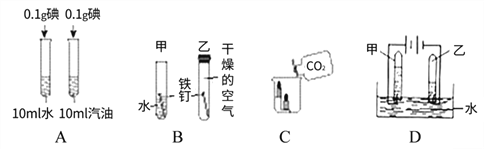
(1)A实验欲探究影响物质溶解性的因素是_______。
(2)B实验说明铁钉生锈与________有关。
(3)C实验得出CO2的性质有_______。
(4)D实验中,甲试管内的气体是_______,该实验得出关于水的组成的结论是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生产生活中具有重要意义,请填空:
(1)写出任一个比较铁比铜活泼的化学方程式_________________________________
(2)某作物叶色发黄,常应施用一定量NH4HCO3,已知碳酸氢铵见光受热易分解,其反应的化学方程式为NH4HCO3![]() NH3↑+CO2↑+X,则X的化学式为________。
NH3↑+CO2↑+X,则X的化学式为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某化学反应微观变化过程的示意图(“![]() ”代表碳原子,“
”代表碳原子,“![]() ”代表氧原子)
”代表氧原子)
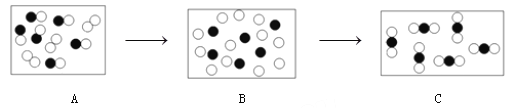
(1)写出图示反应的化学方程式__________________________________________;
(2)该反应中的最小粒子是_________,上图中能表示混合物的是_______(填序号)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国已经全面进入高铁时代,为适应提速要求,需要把短轨焊接成长轨,常用如下反应 XAl + Fe2O3 ![]() XFe + Al2O3 焊接铁轨,该反应发生后不需要持续加热就可保持高温继续进行,方便野外操作,下列说法不正确的是
XFe + Al2O3 焊接铁轨,该反应发生后不需要持续加热就可保持高温继续进行,方便野外操作,下列说法不正确的是
A. 该反应方程式中的X 为3 B. Al2O3 属于氧化物
C. 该反应为置换反应 D. 该反应会放出大量的热
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】草酸(H2C2O4)是生物体的一种代谢产物。下列关于草酸的说法正确的是( )
A. 草酸中氢、碳、氧三种元素的质量比为1:1:2
B. 1个草酸分子中含有1个氢分子、2个碳原子和2个氧分子
C. 180g草酸中氧元素的质量是128g
D. 草酸中所含碳元素的质量分数为![]() ×100%
×100%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学实验小组对 “影响石灰石与盐酸反应速率的因素——盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与。
[进行实验]室温下,选用20mL不同溶质质量分数的盐酸(4%和6%)分别与1g颗粒状或块状的石灰石进行实验(固定夹持仪器略去)。
(1)石灰石与盐酸反应的化学方程式为___________________。
(2)按如图装置进行实验,在装药品前应检查该装置的气密性,具体的做法是____。
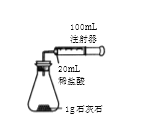
开始实验时,应将20mL稀盐酸_____________(填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中。
[处理数据](3)实验小组进行实验后,获得的相关实验数据如表所示:
实验 编号 | 盐酸的溶质质量分数 (均取20mL) | 石灰石固体形状 (均取1g) | 二氧化碳的体积/mL (均收集前30s的气体) |
a | 4% | 颗粒 | 64.0 |
b | 4% | 块状 | 40.4 |
c | 6% | 颗粒 | 98.2 |
d | 6% | 块状 | 65.3 |
①要比较不同溶质质量分数的盐酸对反应速率的影响,可选择的实验编号是_______(写一组),由此可得到的结论是_______________。
②从上述实验得出石灰石的颗粒大小对反应速率影响的结论是_____________。
(4)如表是实验时记录生成的二氧化碳气体的体积和对应的时间的一组实验数据(每间隔4s读数一次):
时间/s | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 3 | 36 | 40 | |
气体体积/mL | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
从上表数据可以分析得出,到20s后反应速率逐渐变____,其主要原因是___。
(5)你认为影响石灰石与盐酸反应速率的因素还有____,请设计实验方案验证你的猜想:____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种固体物质的溶解度曲线,据图回答下列问题:
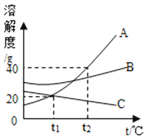
(1)由图可知C物质的溶解度随温度的升高而____(填“增大”、“减小”、“不变”);
(2)t2℃时,140g A物质的饱和溶液中,含有溶质的质量为_____g;
(3)现有t2℃时A、C两种物质的饱和溶液,其饱和溶液中溶质均无剩余,将其均降温到t1℃时,他们的溶质质量分数关系为_____(填序号)。 ①A>C ②A<C ③A=C。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液。同学们对该实验进行了一系列的研究。
探究一:M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:①是______;②是CaCl2。
(2)【设计实验】同学们设计了如下方案并进行实验:
实验操作 | 实验现象 | 实验结论 |
取少量M溶液于试管中,向其中滴加________ | ________________ | 猜想①正确 |
则碳酸钠溶液与M溶液反应的方程式为_____________________。
探究二:过滤后澄清滤液中会有哪些溶质?
(1)【提出猜想】猜想一:NaOH 和Na2CO3;猜想二:__________;猜想三:NaOH。
(2)【实验验证】同学们针对“猜想一”进行了如下实验:
实验操作 | 实验现象 | 实验结论 |
取样于试管中,滴加少量的稀盐酸 | 无气体产生 | 猜想一不成立 |
他们的实验结论是否正确?________,理由是_________________。
(3)【继续探究】设计实验方案确定滤液中溶质的组成。
实验操作 | 实验现象 | 实验结论 |
分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液,B中加入____________溶液 | __________________ | 猜想三成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com