
分析 根据金属活动性顺序可知,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
根据题意,由参加反应的铁的质量,由反应的化学方程式计算出生成铜的质量,进而由质量守恒定律,计算出生成溶液的质量.
解答 解:在金属活动性顺序中,铁在铜的前面,能将硫酸铜中的铜置换为单质铜,同时生成硫酸亚铁,生成的铜为红色金属,覆盖在铁的表面.则:
(1)实验现象是铁丝表面覆盖一层红色物质,溶液由蓝色逐渐变为浅绿色;
(2)化学反应方程式是Fe+CuSO4═Cu+FeSO4;
(3)因为恰好完全反应,故充分反应后溶液中的溶质是硫酸亚铁;
(4)解:设生成铜的质量为x
Fe+CuSO4═FeSO4+Cu
56 64
5.6g x
则$\frac{56}{64}=\frac{5.6g}{x}$,解得x=6.4g
溶液质量为5.6g+200g-6.4g=199.2g.
故答案为:
(1)铁丝表面覆盖一层红色物质,溶液由蓝色逐渐变为浅绿色;
(2)Fe+CuSO4═Cu+FeSO4;(3)D.(4)6.4,199.2.
点评 本题考查了金属活动性顺序的应用,可以依据金属活动性顺序及其意义进行,掌握根据化学方程式的计算、质量守恒定律是正确解答本题的关键.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 冰水混合物、干冰、铁 | B. | 天然气、氯酸钾、钢 | ||
| C. | 石油、石灰石、石墨 | D. | 空气、水、氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | ||
| C. | 2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO | D. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 ,请回答下列问题:
,请回答下列问题: ,W离子的离子符号为Na+;
,W离子的离子符号为Na+;查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 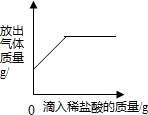 向一定量的石灰石中滴加稀盐酸 | |
| B. |  向一定量过氧化氢溶液中加入少量二氧化锰 | |
| C. | 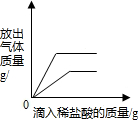 向相同质量的铁粉和锌粉中分别加入足量稀盐酸 | |
| D. |  向一定量硫酸铜溶液中不断加入铁粉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com