
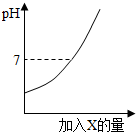
 向盐酸中加入过量某物质X,溶液的pH随加入X的量的变化关系如右下图所示.则X是
向盐酸中加入过量某物质X,溶液的pH随加入X的量的变化关系如右下图所示.则X是

 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
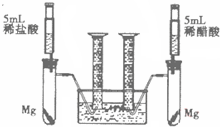 某校化学兴趣小组对金属活动性顺序等知识进行了研究.
某校化学兴趣小组对金属活动性顺序等知识进行了研究.

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验操作 | 测定结果 | 白色固体成分 |
| 用pH试纸测定反应后溶液的酸碱度,操作方法是 用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较. 用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较. |
pH>7 | CaCl2、Ca(OH)2 CaCl2、Ca(OH)2 |
pH≤7 pH≤7 |
CaCl2 |
| OH- | Cl- | SO42- | CO32- | |
| H+ | 溶、挥 | 溶 | 溶、挥 | |
| Ba2+ | 溶 | 溶 | 不溶 | 不溶 |
| Ca2+ | 微溶 | 溶 | 微溶 | 不溶 |
| Mg2+ | 不溶 | 溶 | 溶 | 微溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:
电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有泥沙、Ca2+、Mg2+、Fe3+、SO42-等杂质,不符合电解要求,因此必须经过精制。某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
步聚1:取一定量的粗盐,置于烧杯中,加入足量的水,配成粗盐水;
步聚2:向粗盐水中加入除杂试剂,然后进行过滤,滤去不溶物,再向滤液中加入盐酸调节盐水的pH;
步聚3:将得到的溶液蒸发浓缩、冷却、结晶、过滤、烘干即得精盐;
请回答以下问题:
(1)上述实验中的过滤操作需要烧杯、____________、___________等玻璃仪器。
(2)步聚2中常用Na2CO3、NaOH、BaCl2作为除杂试剂,则加入除杂试剂的顺序为:______________________________________;
(3)步聚2中,判断加入BaCl2已过量的方法是:
________________________________________________;
(4)步聚2中,若先用盐酸调节pH再过滤,将会对实验结果产生影响,其原因是:
________________________________________________;
(5)为检验精盐纯度,需配制150 mL 0.2 mol/L NaCl(精盐)溶液,上图是该同学转移溶液的示意图,图中的错误是___________________、_____________________。
查看答案和解析>>
科目:初中化学 来源:《第7章 应用广泛的酸、碱、盐》2010年单元测试卷(2)(解析版) 题型:解答题
| 实验步骤 | 实验现象 | 结论、解释与化学方程式 |
| 1、向一定量的盐酸中加入铝片 | 有_____________出现 | 化学方程式: _____________________ |
| 2、向上述正在反应中的溶液里逐滴加入NaOH溶液 | 产生气泡的速度逐渐减慢;一段时间后,溶液中没有气泡放出. | 原因:_______________ 化学方程式:__________ 结论:_______________ |
| 3、继续向上述溶液中滴加NaOH溶液 | 溶液中又开始有气泡生成 | ------------------ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com