
 2MgO;基本反应类型是化合反应;
2MgO;基本反应类型是化合反应;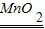 2H2O+O2↑,该反应为放热反应;
2H2O+O2↑,该反应为放热反应; 2MgO;化合反应
2MgO;化合反应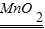 2H2O+O2↑,放热;
2H2O+O2↑,放热;

 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源:2010年江苏省苏州市昆山市中考化学一模试卷(解析版) 题型:填空题
查看答案和解析>>
科目:初中化学 来源:2010年江苏省苏州市昆山市中考化学一模试卷(解析版) 题型:填空题
| 温度/℃ | 20 | 40 | 60 | 80 | 100 | ||
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
| Ca(OH)2 | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 | 0.07 |
查看答案和解析>>
科目:初中化学 来源:2010年中考化学辅导跟踪练习试卷(8)(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com