
| A. | 5g | B. | 3g | C. | 8g | D. | 11g |
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:初中化学 来源: 题型:解答题
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
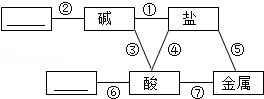 归纳是学习化学的重要方法,总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白:
归纳是学习化学的重要方法,总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入稀硫酸的质量 (g) | 5 | 5 | 5 | 5 | 5 |
| 生成氢气的质量(g) | 0.02 | 0.04 | m | 0.08 | 0.08 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 石墨具有优良的导电性能,可用来做电极 | |
| B. | 硝酸铵固体溶解时放热 | |
| C. | 合金硬度一般比组成它的纯金属大 | |
| D. | SO2、CO、NO2都是造成空气污染的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
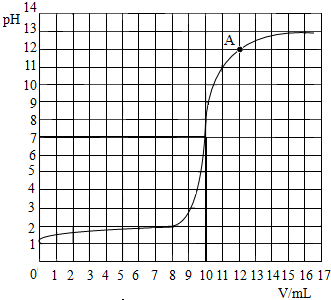 在盛有10克稀盐酸的烧杯中,逐滴滴加溶质质量分数为4%的氢氧化钠溶液,反应过程中不断搅拌并及时用pH计(一种测定溶液pH的仪器)测定溶液的pH,烧杯中溶液的pH与加入氢氧化钠溶液体积(V)之间的变化关系如图所示.
在盛有10克稀盐酸的烧杯中,逐滴滴加溶质质量分数为4%的氢氧化钠溶液,反应过程中不断搅拌并及时用pH计(一种测定溶液pH的仪器)测定溶液的pH,烧杯中溶液的pH与加入氢氧化钠溶液体积(V)之间的变化关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com