
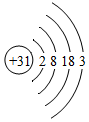
 ,在元素周期表中镓元素位于第四周期,镓原子失去电子形成离子的符号可表示为Ga3+.
,在元素周期表中镓元素位于第四周期,镓原子失去电子形成离子的符号可表示为Ga3+.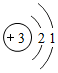 B.
B.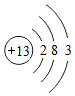 C.
C.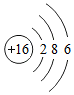 D.
D.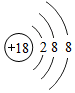
分析 (1)天然气的主要成分是甲烷(CH4),甲烷在点燃条件下燃烧生成二氧化碳和水,写出反应的化学化学方程式即可.
(2)根据化肥的分类进行分析;
(3)①根据电子层数和周期数相同解答;
②根据元素周期表的信息以及最外层电子数决定元素的化学性质来分析.
解答 解:
(1)天然气的主要成分是甲烷(CH4),甲烷在点燃条件下燃烧生成二氧化碳和水,反应的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)含有氮元素的肥料称为氮肥,尿素中含有氮元素,是一种氮肥.故填:氮.
(3)①由镓元素(Ga)的原子结构示意图可知:原子核外有4个电子层,在元素周期表中镓元素位于第四周期,镓原子最外层电子数为3,易失去3个电子,形成离子的符号可表示为:Ga3+;
②由元素周期表的信息可知,最外层电子数决定元素的化学性质,最外层电子数相同化学性质相似,镓原子的最外层有3个电子,所以与B原子的最外层有3个电子,所以二者化学性质相似;
故填:B.
答案:
(1)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(2)氮;
(3)①四;Ga3+;②B.
点评 此题所考查知识点较多较细,在解答时要明确题目所需解决的问题,善于联系所学知识并迁移到该题进行解答.


科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铜有良好的导电性,常用于制作导线 | |
| B. | 所有的金属都能与稀盐酸反应 | |
| C. | 铁制品在干燥的空气中不易生锈 | |
| D. | 不锈钢具有较强的耐腐蚀性,可用于制作医疗器械 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
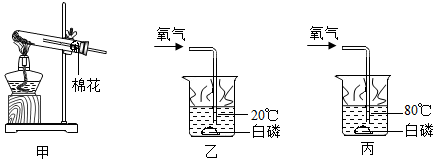
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 该反应属于复分解反应 | |
| B. | 反应前后分子种类和数目不变 | |
| C. | 甲物质中氮、氢元素的质量比为1:3 | |
| D. | 参加反应甲、乙物质的分子个数比为4:5 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
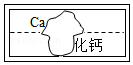 在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于 试管中,向其中滴加酚酞溶液. | 酚酞溶液变红色. | 猜想①正确,碳酸钠与其反应的化学 方程为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH. |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气体产生. | “猜想一”不成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
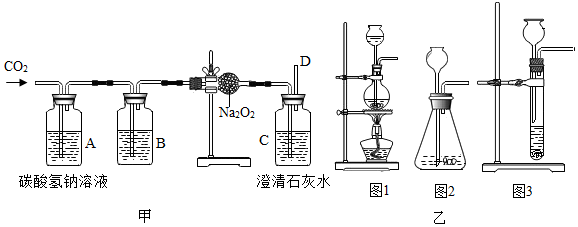
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 预期现象和必要结论 |
| 步骤:1:取少量样品于烧杯中,缓慢加入足量蒸馏水,充分搅拌,静置,过滤. | 得到无色溶液 |
| 步骤2:取少量步骤1所得的滤液于试管中,加入过量稀盐酸,振荡后静置. | 有气泡产生. |
| 步骤3:取少量步骤2所得的溶液于试管中,滴加少量的BaCl2溶液. | 有白色沉淀生成,说明样品中有MgSO4. 无明显现象,说明样品中没有MgSO4. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com