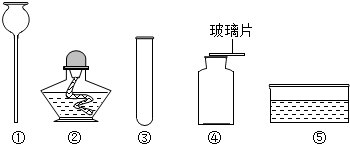
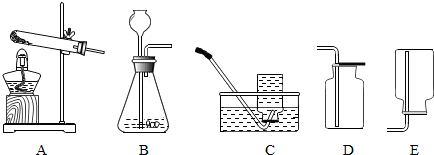
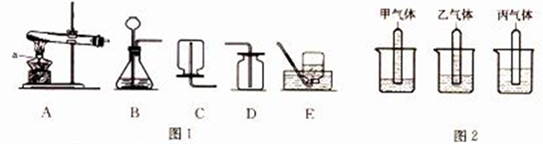
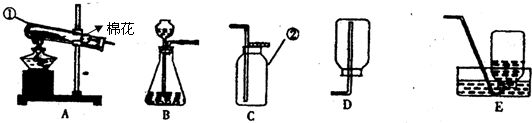
解:(1)仪器名称为:铁架台、长颈漏斗
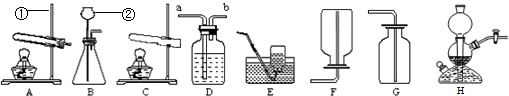
(2)氯酸钾和二氧化锰是固体,反应条件是加热,故发生装置需选择A,氧气不易溶于水,密度比空气大,可用排水法或向下排空气法收集.因此装置组合为:AD或AE、AG;反应的化学方程式为:2KClO
3
2KCl+3O
2↑
(3)通入氧气将水排出,氧气需从短管进,水从长管排出
(4)反应物是块状固体和液体,且无需加热,故可用H装置制取硫化氢气体.
(5)氢气还原氧化铜,氢气需通到试管底部将空气全部排出,故A装置可进行这样的改进:试管塞子拿掉,换成长导管伸到接近试管底部,化学方程式为:H
2+CuO

Cu+H
2O
(6)根据图象可知氧气的质量为0.48g,根据化学方程式氧气的质量,可求出过氧化氢的质量,从而求出过氧化氢溶液的溶质质量分数.
故答案为:
(1)铁架台、长颈漏斗
(2)AD或AE、AG,2KClO
3
2KCl+3O
2↑
(3)a
(4)能,反应物是块状固体和液体,且无需加热
(5)试管塞子拿掉,换成长导管伸到接近试管底部.H
2+CuO

Cu+H
2O
(6)解:设:有过氧化氢的质量为x参加反应
2H
2O
2
2H
2O+O
2↑
68 32
X 0.48g
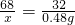
X=1.02g
双氧水溶液中溶质质量分数=

×100%=2%
答:该溶液中双氧水的溶质质量分数是2%.
分析:根据反应物和反应条件选择发生装置,根据气体的密度和溶解性选择收集装置;根据反应物和生成物写出化学方程式,根据化学方程式中已知物质的质量可求出待求物质的质量.
点评:明确发生装置和收集装置的选择依据,会根据化学方程式进行简单计算.

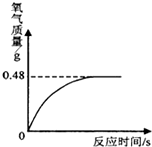 则该溶液中双氧水的溶质质量分数是多少?
则该溶液中双氧水的溶质质量分数是多少? 2KCl+3O2↑
2KCl+3O2↑ Cu+H2O
Cu+H2O 2KCl+3O2↑
2KCl+3O2↑ Cu+H2O
Cu+H2O 2H2O+O2↑
2H2O+O2↑ 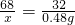
 ×100%=2%
×100%=2% 

 阅读快车系列答案
阅读快车系列答案
 则该溶液中双氧水的溶质质量分数是多少?
则该溶液中双氧水的溶质质量分数是多少?