
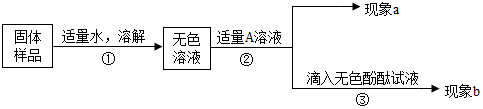
分析 由题目给出的信息和学过的知识可知:已知空气中的二氧化碳与氢氧化钠反应生成碳酸钠和水;因此做出的猜想是:猜想Ⅰ.全部是NaOH;猜想Ⅱ.全部是Na2CO3;猜想Ⅲ.Na2CO3和NaOH的混合物;若现象a为有气泡产生,则加入的A溶液是稀盐酸或稀硫酸,说明氢氧化钠已经变质,碳酸钠和盐酸反应生成氯化钠和水和二氧化碳,配平即可;若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为碳酸钙,该实验不能说明样品中有氢氧化钠,因为碳酸钠和氢氧化钙反应会生成氢氧化钠;若A是氯化钙溶液,现象a有白色沉淀产生,现象b无色酚酞不变红色,则猜想Ⅱ成立,因为碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,氯化钠显中性;如果现象a有白色沉淀产生,现象b无色酚酞变红色,则猜想Ⅲ成立;氢氧化钠变质是因为与空气中的二氧化碳反应生成了碳酸钠和水,据此解答.
解答 解:猜想Ⅲ:已知空气中的二氧化碳与氢氧化钠反应生成碳酸钠和水,因此做出的三个猜想是:全部是NaOH;全部是Na2CO3;Na2CO3和NaOH的混合物;故答案为:Na2CO3和NaOH的混合物;
【实验和推断】(1)若现象a为有气泡产生,则加入的A溶液是稀盐酸或稀硫酸,说明氢氧化钠已经变质,故答案为:稀盐酸;
(2)若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为碳酸钙,该实验不能说明样品中有氢氧化钠,因为碳酸钠和氢氧化钙反应会生成氢氧化钠;故答案为:不能;
(3)若A是氯化钙溶液,现象a有白色沉淀产生,现象b无色酚酞不变红色,则猜想Ⅱ成立,因为碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,氯化钠显中性;故答案为:有白色沉淀产生,无色酚酞不变红色;
【反思】久置的氢氧化钠变质的原因是:空气中的二氧化碳与氢氧化钠反应生成碳酸钠和水,故答案为:CO2+2NaOH=Na2CO3+H2O.
点评 本考点既考查了探究氢氧化钠是否变质,又考查了实验步骤的设计和化学方程式的书写,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是实验室用加热高锰酸钾的方法制取氧气的装置图,请回答下列几个问题:
如图是实验室用加热高锰酸钾的方法制取氧气的装置图,请回答下列几个问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | H2SO4属于酸 | B. | CO32-属于酸 | C. | NO3-属于碱 | D. | Na+属于碱 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
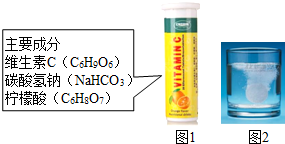 气泡产生(如图2).该小组同学进行如下探究.
气泡产生(如图2).该小组同学进行如下探究.| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验 序号 | 实验目的 | 实验方案 | 实验现象 | 结论 |
| 实验1 | 探究草木灰的成分 | 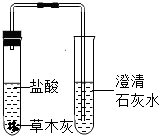 | ①有气泡产生 ②石灰水变浑浊 | 草木灰的主要成分是碳酸钾 |
| 实验2 | 探究碳酸钾的性质 | 向碳酸钾溶液中滴入澄清石灰水 | 有白色沉淀生成 | 化学方程式为K2CO3+Ca(OH)2=CaCO3↓+2KOH |
| 实验3 | 探究实验2反应后上层清液中溶质的成份 | 滴入澄清石灰水 | 有沉淀生成 | 上层清液中有两种溶质 KOH和K2CO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com