������NH
3����ͨ��״������һ���д̼�����ζ�����壬�ܶȱȿ���С����������ˮ����ˮ��ҺΪ��ˮ��ʵ���ҿ��ü����Ȼ�狀���ʯ�����ֹ�������ķ�����ȡ������
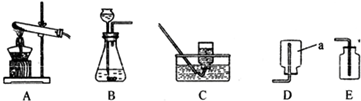
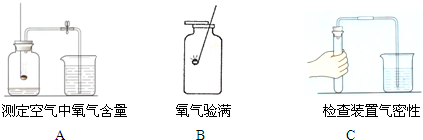
��1��ʵ������ȡ������ѡ�ó��л�ѧ����ȡ
����
����
�ķ���װ�ã�������
��Ӧ���״̬�ͷ�Ӧ�������ڹ��������
��Ӧ���״̬�ͷ�Ӧ�������ڹ��������
��
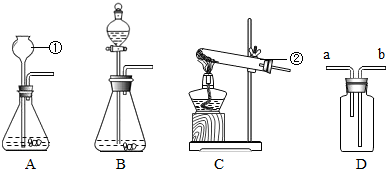
��2��������һ���Լ��Ե����壬Ϊ��֤������������һ��������ʱ��Ҳ�Ǿ��л�ԭ�Ե�һ�����壬ʵ��װ������ͼ��

������ͨ��װ��ij�ֺ�ɫ��ĩ�IJ����ܣ�A���У����ȣ�����ɫ��ĩȫ��ת���ɹ����ĺ�ɫ��ĩʱ��U�ܣ�B���Ĺ�������ɫ��ͬʱ����ƿ��C�����ռ���һ����ɫ��̬����X��ʵ�����������±���
|
��������ʵ�����顡��ǰ |
��������ʵ�����顡���� |
| ��������ɫ��ĩ+������ |
��������65.6g |
��������59.2g |
| ��������ˮ����ͭ+U�ι� |
��������100.8g |
��������108.0g |
�ش��������⣺
�٣�A���з�Ӧ�Ļ�ѧ����ʽΪ
��
�ڵ���X����ˮ���ռ�������
������������ˮ
������������ˮ
��
��ȡ�ӣ�C�����ų���ˮ1��2ml�����Թ��У�����1��2ml��ɫ��̪��Һ����Һ��
��
��
ɫ����������
δ��ȫ��Ӧ�İ������浪���ų�������ˮ�Լ��ԣ�����Һʹ��̪��Һ���
δ��ȫ��Ӧ�İ������浪���ų�������ˮ�Լ��ԣ�����Һʹ��̪��Һ���
��
�ܼ�����b�������ų���β���к��������İ�����������ˮ�����ķ����⣬������
����
����
��Һ���д��������ⰱ��Ⱦ������
���ڴ˷�Ӧ�У����ɹ����ĺ�ɫ���ʵ�����Ϊ
25.6
25.6
g��




 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�