
【题目】化学反应前后肯定发生变化的是( )
A.原子数目 B.原子质量 C.元素种类 D.物质种类
科目:初中化学 来源: 题型:
【题目】将铁粉和铜粉混合物7.0g,加入到盛有60.0 g稀盐酸的烧杯中,恰好完全反应。此时烧杯内各物质的总质量为66.8 g。试计算:
(1)原混合物中铁粉的质量分数。(精确到0.1%)
(2)反应后所得溶液中溶质的质量分数。(精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳还原氧化铜的实验装置。某化学小组对该实验及产物的探究如下:
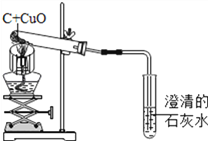
【分析】
(1)写出该反应的化学方程式_______________________。
(2)酒精灯加网罩的目的是_________________________。
(3)刚开始加热时,澄清石灰水中有气泡冒出,但澄清石灰水不变浑独,原因是_______________。
(4)实验结束应先_________。(选填答案序号)
A.撤离酒精灯 B.将导管移出石灰水. C.拨掉橡胶塞
【探究一】检验产物成分
【提出问题】:实验产物是暗红色固体,很难观察到紫红色固体,暗红色固体是什么?
【查阅资料】:氧化亚铜(Cu2O)为红色固体;Cu2O+H2SO4 =CuSO4 +Cu + H2O。
【猜想与假设】:暗红色固体除铜外还可能含有Cu2O
【设计实验】
(5)操作:取少量暗红色固体,加入稀硫酸,观察到现象:___________、_____________。结论:暗红色固体含有Cu2O。
【探究二】测定产物中Cu2O的含量
(6)为测定红色固体中氧化亚铜的质量分数,小组同学设计了如下两种方案:
甲方案:甲同学称取10g红色固体加人到足量稀硫酸中使其充分反应后,过滤_______(填操作名称)、干燥、称量剩余红色固体的质量为8 g,则红色固体中氧化亚铜的质量分数为__________。
乙方案:实验原理:Cu2O +H2![]() 2Cu +H2O,称取一定质量的固体样品,用如图装置进行实验(固定装置略,碱石灰为氧化钙和氢氧化钠的混合物,通过测定反应前后装置d的质量达到实验目的。
2Cu +H2O,称取一定质量的固体样品,用如图装置进行实验(固定装置略,碱石灰为氧化钙和氢氧化钠的混合物,通过测定反应前后装置d的质量达到实验目的。
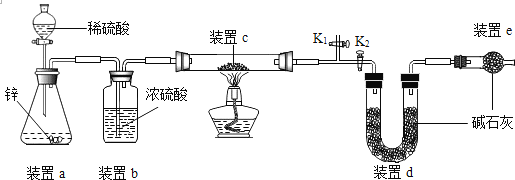
(7)装置a中用稀硫酸而不用稀盐酸,原因是_______________;
(8)若不加装置c,实验结果会偏_______(“大”或“小”),原因是_______________;
(9)点燃酒精灯前涉及的部分操作如下,正确的顺序是_____________;
①打开K2,关闭K1 ②检查装置的气密性 ③连接仪器 ④关闭K2,打开K1,通氢气一段时间
【拓展反思]】:
(10)还可通过测定反应前后装置________(填“a”、“b”、“c”)的质量达到测定产物中Cu2O的含量目的。
(11)乙方案第(9)的④中“通氢气一段时间”的目的是排出装置内的空气,否则可能带来哪些影响?__________、_____________(答出两点)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】抗甲型H1N1流感的有效药物“达菲”可用莽草酸(化学式C7H10O5)制取.有关莽草酸的说法中正确是( )
A.该物质是由22个原子构成的
B.其中氢元素的质量分数最大
C.氢、氧元素的质量比为2:1
D.完全燃烧后的产物是CO2和H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)某研究人员按下图所示流程进行“燃煤烟气的脱硫研究”。实验中,SO2和O2
的混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环。
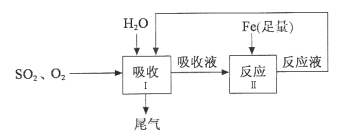
(1)Ⅰ中发生反应的化学方程式是2SO2+2H2O+O2 2X,则X的化学式是 。
(2)Ⅱ中发生反应的化学方程式是 。
(3)随着反应液流入Ⅰ中,吸收液中X的生成速率明显加快,其原因可能是 。
(4)经过多次循环后,反应液可以用来制备FeSO4·7H2O,它在医疗上常用于治疗
(选填字母)。
A.甲状腺肿大 B.佝偻病 C.龋齿 D.贫血症
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】石墨烯是“新材料之王”。它是由碳原子构成、且只有一层原子厚度的晶体。它是目前发现的最薄、强度最大、导电导热性能最好的材料。下列物质中与石墨烯的组成元素完全相同的是( )
A. 金刚石 B. 干冰 C. 碳酸钙 D. 一氧化碳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)某市热电厂使用的燃料是含硫较多的煤.该厂附近一所中学的同学经常闻到空气有异味,且空气能见度差.学习化学后,同学们意识到这有可能是该厂排出的废气超标造成的,于是在老师的指导下做了探究实验,请你填写下列空白,
【提出问题】该厂附近所降雨水是否是酸雨?空气里SO2是否超标呢?
【查阅资料】I.我国关于SO2在风景区、居民区、工厂区的空气质量最高标准分别见下表:
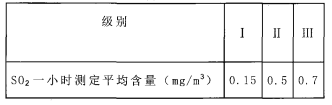
Ⅱ.硫酸钡既不溶于水,也不溶于酸(如不与稀盐酸、稀硝酸等反应).
【设计实验1】第一组同学取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示:

所降雨水 (填“是”或“不是”)酸雨。在测定时间内酸雨pH减小的原因可能是__
【设计实验2】第二小组同学设计以下步骤来测定空气中SO2的含量.
(1)用2L的空可乐瓶采集工厂附近的空气样品,采样的具体操作是:
(2)向取回的装有空气样品的可乐瓶中倒入NaOH溶液,盖紧瓶塞后充分振荡,仿照CO2与NaOH溶液的反应,写出SO2与NaOH溶液反应的化学方程式:
(3)加入一定量氧化剂H2O2,使其中Na2SO3完全转化为Na2SO4.向可乐瓶中加入过量的BaCl2溶液.Na2SO4和BaCl2反应的化学方程式为: ____
(4)经过过滤、洗涤、烘干,称量固体质量为1.165mg.
计算:1.165mg硫酸钡中硫元素的质量为 mg.由质量守恒定律可知,2L空气样品中SO2的质量为 mg.
由空气质量标准可得出结论:该厂排放的SO2严重超标.。
【发现新问题】考虑到空气中的各种气体成分,第一组认为第二组同学的SO2的含量偏大,其依据是 ;你提出的实验改进方案是
【反思与应用】为尽快改善该地区的空气质量,请你提出一条合理化建议:
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)人类的生活和生产都离不开金属材料。

(1)铁锅、铝锅是生活中常用的炊具,下图是铁锅的示意图。
铁锅生锈的条件是:铁与空气和__________直接接触;炒菜时铁锅中的油着火可用锅盖盖灭,其原理是____________________________。铝锅轻便、耐用,其原因是 。
(2)某同学为了验证镁、铁、铜的活动性顺序,他选择了打磨过的铁丝,你认为他还需要的另外两种溶液是________ _____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com