


 ѧϰʵ����ϵ�д�
ѧϰʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��OH����Na+��K+ | B��SO42����Cu2+��K+ |
| C��K+��Cl����NO3�� | D��Ca2+��NH4+��CO32�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢� | B���ڢۢ� | C���ۢ� | D���ڢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CaCO3��Ca(OH)2 | B��CO2��O2 | C��H2SO4��H2O | D��Fe��Cu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaOH�������ƴ��� | B��NaHCO3 ̼�������մ� |
| C��C2H5OH�Ҵ��ƾ� | D��CaO��������ʯ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
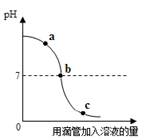
| A����ʵ���ǽ�����������Һ���������� |
| B��b���ʾ�������������ǡ����ȫ��Ӧ |
| C��a��ʱ����Һ��ʹʯ����Һ��� |
| D��c��ʱ����Һ�У�����ֻ���Ȼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ϡ����������к�ӡȾ���ļ��Է�ˮ |
| B���ռ�����ڵ������������� |
| C��̼�����ƿ����ڱ��Ƹ�� |
| D���Ȼ��ƿ�����������·��ѩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
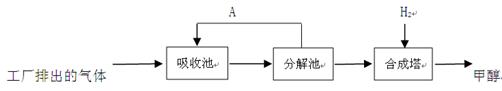
| A���÷������Լ���̼�ŷ� | B����ѭ�����õ�����A��K2CO3 |
| C���ֽ���е���Ҫ��Ӧ���ڷֽⷴӦ | D���ϳ����е���Ҫ��Ӧ���ڻ��Ϸ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com