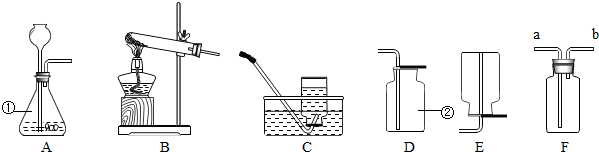
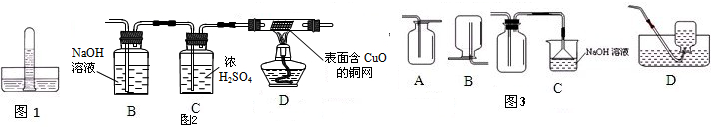
某班同学在实验室进行二氧化碳的制取和性质实验,发现实验桌上已摆放了如下图所示的仪器可供选用:
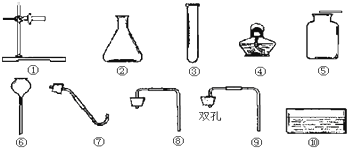
(1)要制取大量的CO
2,反应过程要便于添加液态的反应物,组合一套符合要求的装置来制取CO
2,你选用的仪器组合是
②⑥⑨
②⑥⑨
(填序号).
(2)下列是同学们对实验室制取CO
2药品选择的讨论,你认为正确的是
①②④
①②④
(填序号)
①不能用浓盐酸,因为浓盐酸易挥发,使氯化氢气体混入二氧化碳气体中.
②一般不选用碳酸钠粉末,因为它与酸反应速度太快,不便于收集.
③可用木炭和氧气反应,因为反应可生成二氧化碳.
④可用稀盐酸与石灰石反应,因为反应速度适中,条件要求不高,气体产物纯净,易于收集.
(3)将集满CO
2气体的试管倒插入水中并轻轻振荡试管,可观察到的现象是
试管中液面上升
试管中液面上升
,该现象说明CO
2具有的性质是
溶于水
溶于水
.
(4)用制取二氧化碳的气体发生装置还可以制取其它气体.请举出一例:可制取的气体是
氧气
氧气
,制气反应的化学方程式是
,可用制二氧化碳的装置制该气体的理由是
该反应为固体和液体不需加热的反应,与制二氧化碳的反应物状态和条件相同故可用制二氧化碳的装置
该反应为固体和液体不需加热的反应,与制二氧化碳的反应物状态和条件相同故可用制二氧化碳的装置
.
(5)以上仪器也可用于实验室制取氨气.实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH
3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,其水溶液呈碱性.
①制取氨气反应的方程式:2NH
4Cl+Ca(OH)
2CaCl
2+2NH
3↑+2X.X的化学式为:
H2O
H2O
.
②实验室制取并收集NH
3,可以从上图中选择仪器进行组装,除选择①③⑤外,还必须用到的仪器是
④
④
(填序号).
③NH
3是一种碱性气体,干燥时不能选用下列干燥剂中的
B
B
(填字母).
A.固体氢氧化钠 B.浓硫酸 C.生石灰.

 阅读快车系列答案
阅读快车系列答案