
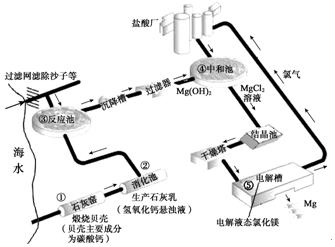
分析 根据已有的反应的类化学方程式的书写、加热蒸发溶质质量分数的变化以及海水资源的利用进行分析解答即可.
解答 解:(1)据图可以看出,①是碳酸钙高温分解生成氧化钙和二氧化碳,②是氧化钙和水发生化合反应,③是氢氧化钙和氯化镁发生复分解反应,④是氢氧化镁和盐酸发生复分解反应,⑤是氯化镁分解生成镁和氯气,故填:①⑤;
(2)氢氧化镁和盐酸反应生成氯化镁和水,故填:2HCl+Mg(OH)2=MgCl2+H2O;
(3)MgCl2溶液在进入结晶池之前需先加热浓缩,加热过程中,MgCl2溶液中溶质质量分数会由于水分的减少而增大,故填:增大;
(4)海水中的资源很多,可以利用海水晒盐、淡化海水,故填:海水晒盐.
点评 本题考查的是海洋资源的利用,完成此题,可以依据已有的知识进行.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 根据质量守恒定律,可确定参加反应的各物质的质量比 | |
| B. | 根据“酸、碱和盐溶解性表”,可以帮助判断复分解反应能否发生 | |
| C. | 根据金属活动性顺序,可以判断金属能否与稀盐酸、稀硫酸发生置换反应 | |
| D. | 根据物质溶解度曲线图,可确定该物质在某一温度时溶液中溶质与溶剂的质量关系 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 晚上,静静和妈妈一起做晚饭.
晚上,静静和妈妈一起做晚饭.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com