
分析 (1)根据提示的反应以及对应的现象结合加入的少量铁粉等要素分析;
(2)①根据固体变化情况分析;
②根据给出的数据结合对应的化学方程式计算.
解答 解:
(1)根据①2FeCl3+Fe═3FeCl2 ②CuCl2+Fe═FeCl2+Cu以及对应的现象可知,铁参加了反应,但是却没有得到铜,说明先发生的是第一个反应,结果铁的质量很少,导致没机会和氯化铜反应,从而没有得到铜;
(2)①2FeCl3+Fe═3FeCl2 这个方程式时固体减少的反应; ②CuCl2+Fe═FeCl2+Cu这个反应加入56g铁就生成64g的铜,是固体增加的反应.当第一个的减少量和第二个的增加量相等时,固体沉积物质量与加入铁粉质量相等.
②设反应②消耗的铁的质量为y.反应②导致的固体增加量为a
CuCl2+Fe═FeCl2+Cu 固体增加量
56 64 64-56=8
y 1.6g a
$\frac{56}{y}$=$\frac{64}{1.6g}$=$\frac{8}{a}$
y=1.4g
a=0.2g
由于固体沉积物质量与加入铁粉质量相等,也就是铜的质量等于加入的全部的铁的质量,所以1.6g-1.4g=0.2g.
或者根据第一个反应固体减少量为加入的铁的质量,等于第二个反应的固体增减量0.2g,所以第一个反应消耗的铁的质量为0.2g.
故答案为:
(1)加入的铁先和氯化铁反应,由于铁的量不足,没有来得及和氯化铜反应;
(2)①铁和氯化铁反应固体质量是减少的,而铁和氯化铜反应固体质量是增大的,当两者变化量相同时则固体沉积物质量和加入的铁质量相等;
②0.2g; 1.4g.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:初中化学 来源: 题型:填空题
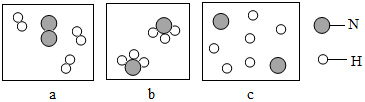
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
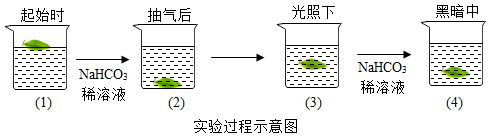
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 甲、乙、丙 | B. | 甲、乙、丁 | C. | 甲、丙、丁 | D. | 乙、丙、丁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.安全知识 | B.生活常识 |
| ①给试管里的液体加热时--试管口不要对着人 ②浓硫酸沾到皮肤上--用水冲洗后涂上硼酸溶液 | ①铁锅表面保持清洁干燥防止生锈 ②用铅笔芯粉末使铁锁开启灵活 |
| C.除去杂质 | D.元素与人体健康 |
| ①用稀盐酸除去铜粉中的少量氧化铜粉末 ②滴加氯化钙溶液除去烧碱溶液中的少量碳酸钠 | ①缺氟--会引起氟斑牙和氟骨病 ②吃水果、蔬菜--可以补充维生素 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
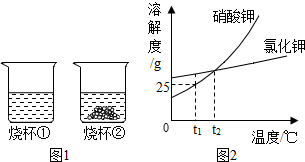 t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示.则下列说法正确的是( )
t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示.则下列说法正确的是( )| A. | 烧杯①的溶液一定是不饱和溶液 | |
| B. | 烧杯①的溶液是硝酸钾溶液 | |
| C. | 若烧杯②的溶液升温到t2℃时,烧杯底部还有部分物质不溶解 | |
| D. | 若将烧杯①和烧杯②的溶液都升温到t2℃时,溶质的质量分数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com