
【题目】同学们通过学习金属后,对铜的化学性质进行了进一步的研究。
项目一. 同学们将光亮铜片放在酒精灯火焰上灼烧,发现表面变黑,他们对黑色物质来源产生了兴趣,铜片表面黑色物质是什么呢?
【查阅资料】
(1)酒精不充分燃烧产生炭黑(即黑烟);
(2)氧气的化学性质比较活泼,加热条件下能与金属铜反应生成黑色的氧化铜。
(3)氧化铜能与硫酸反应生成硫酸铜和水;炭黑难溶于水,且与硫酸不发生反应。
【猜想与假设】
猜想1:黑色固体是炭黑。
猜想2:黑色固体是空气中的氧气与铜反应生成的氧化铜。
猜想3:黑色固体既有炭黑又有氧化铜。
【进行实验】
实验步骤和方法 | 实验现象 | 实验结论 |
实验一:取一小段光亮铜片,放入试管内,然后用试管夹夹持试管,放在酒精灯的外焰部位加热。 | 铜片变黑 | (1)猜想1不正确。 (2)黑色固体可能与空气中的 ______ 有关。 |
实验二:取一试管,将一小段光亮铜片放入试管中,塞上胶塞,并用注射器抽出试管内的空气,封好胶塞,并加热,观察现象。趁热取下胶塞,观察现象。 | ________ | 猜想2正确 |
实验三:将在酒精灯火焰上灼烧后的附着黑色固体的铜片,投入到盛有稀硫酸的试管中。 | ________ | 猜想3不正确 |
项目二. 同学们通过学习知道铜与盐酸、稀硫酸不能发生反应,但却发现化学老师用铜与硝酸制备出气体去做物理实验。同学们在实验室对铜与稀硝酸的反应进行了探究。
实验I | |
实验装置 | 实验现象 |
| 铜片逐渐消失, 有无色气泡产生,试管中上部有红棕色气体出现; 溶液由无色变为蓝色 |
【探究】实验I中产生的无色气体是什么?
【查阅资料】
(1)硝酸(HNO3)与Cu反应生成硝酸铜和含氮元素的化合物;硝酸铜溶液呈蓝色;
(2)氨气(NH3)可以使酚酞溶液变红
(3)含氮元素的某些气态物质的物理性质
NH3 | NO | NO2 | |
颜色 | 无色 | 无色 | 红棕色 |
气味 | 刺激性 | 刺激性 | |
溶解性 | 极易溶于水 | 难溶于水 | 可溶于水或硝酸 |
【猜想与假设】无色气体可能是:①NH3 ②NO
【进行实验】同学们利用下图装置对产生的无色气体进行检验。
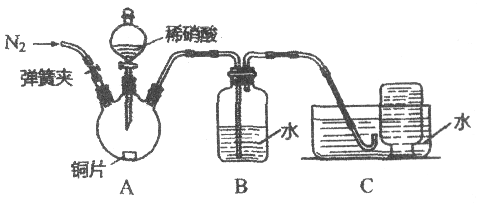
实验操作 | 实验现象 |
1. 打开弹簧夹,通入N2,一段时间后,关闭弹簧夹 | B、C中导管口有无色气泡冒出 |
2. 将C中导管伸入集气瓶中,打开分液漏斗的活塞,滴入一定量稀硝酸,关闭活塞 | A中有无色气泡产生 B中导管口有无色气泡冒出 C中集气瓶内收集到无色气体 |
3. 从水槽中取出集气瓶,敞口置于空气中 | 无色气体变为红棕色 |
4. 取少量B中液体于试管中,滴加无色酚酞溶液 | 试管中溶液颜色无明显变化 |
【解释与结论】
(1)操作1中,通入N2的目的是__________。
(2)同学们认为猜想①不正确,理由是__________。
(3)无色气体具有的化学性质是__________。
【答案】 氧气 打开胶塞前铜片不变黑,打开胶塞后铜片变黑 黑色固体全部溶解,溶液由无色变为蓝色 排出装置中的空气,防止干扰 B中液体加酚酞溶液不变色,说明不是氨气 能与氧气反应
【解析】(1)铜与空气中的氧气接触,在加热的条件下变为黑色,故可能与空气中的氧气有关;
(2)刚开始,试管中的氧气被抽空,铜没有变黑,当打开试管时,炽热的铜与空气中的氧气接触,铜变为黑色,说明铜在空气中加入生成了氧化铜;
(3)猜想3不正确,说明没有炭黑,只有氧化铜生成,故加入稀硫酸后可以看到的现象是黑色固体全部溶解,溶液由无色变为蓝色
(4)操作1中,通入N2的目的是排出装置中的空气,防止干扰;
(5)B中液体加酚酞溶液不变色,说明不是氨气;
(6)无色的气体遇到氧气时生成了红棕色的二氧化氮气体,说明该气体能与氧气反应;


科目:初中化学 来源: 题型:
【题目】M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动.
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是 。
【设计与实验一】小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有体积相同、溶质质量分数也相同的稀盐酸);
实验操作 | M丝插入试管①中 | 钢丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu: |
几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 |
|
【交流与表达】同学们对同一实验得出两种不同结论的现象进行了讨论,明白了实验刚开始时试管③中无气泡产生的原因,该原因是 。
【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:
(1)试管乙中观察到的现象是 。
(2)试管丙中反应的化学方程式为 。
【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管 (填试管编号)中的实验,也可以得出正确的结论。
【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序。
【评价与反思】实验结束后,同学们对实验过程进行了如下反思:

(1)影响金属与酸反应速率快慢的因素,除了相互反应的金属和酸的性质外,还有 (任写一种)
(2)探究金属活动性顺序时,除了上述实验中已经用到的两种方法外,还可以根据 进行判断(任写一种)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示。下列说法正确的是( )
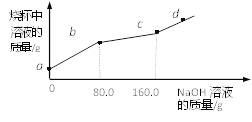
A. ab段反应产生蓝色沉淀
B. bc段溶液增加70.2g
C. c点对应的溶质质量分数为4.9%
D. d点溶液显碱性
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组对某品牌牙膏中碳酸钙含量进行以下探究。该牙膏摩擦剂主要由碳酸钙、氢氧化铝组成,其他成分遇到盐酸时无气体生成。现利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定B中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。请回答下列问题。(已知:碱石灰固体的主要成分是生石灰和烧碱)

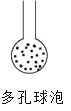
(1)装置A中牙膏样品放置在_______(填仪器名称)中,盐酸放置在装置______(填仪器名称)中,A中至少发生___(填数字)个反应,写出其中一个反应的化学方程式______
(2)若测定值比实际值小,可能的原因有________________(填字母)
a.装置A中水蒸气、HCl等进入装置B中
b.装置A中CO2未完全进入装置B
c.CO2气流速度太快导致Ba(OH)2未完全吸收
d.盐酸未滴加过量
(3)为减少误差,现采取以下一些措施:
①在A、B之间增加一个装有_____(填化学式)溶液的洗气瓶,它的作用是___;
②若将装置B中的长导管下方增加一个多孔球泡,作用是___;
③若将装置A的前面再增加一个鼓入氮气的装置,目的是_____________;
④若在装置B的后面再增加一个装有碱石灰固体的干燥管,目的是___________________
(4)准确称取三份各16.00g的样品,进行测定,测得BaCO3质量分别为3.96g、3.92g、3.94g。请计算样品中碳酸钙的质量分数。(写出计算过程)_______
(5)某同学利用上述方法测定牙膏中钙元素的质量分数。小李同学认为即使即使排除实验仪器和操作的影响,上述测定的结果仍有可能偏小,理由是:
_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验小组同学在实验室制取二氧化碳,并验证二氧化碳的化学性质。
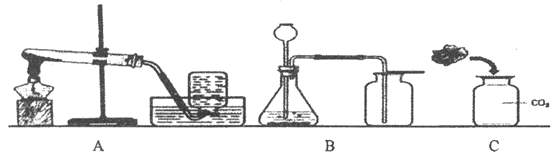
(1)实验室用大理石和稀盐酸制取二氧化碳的化学方程式为________,应选用的装置是________(填序号);收集二氧化碳时,检验集气瓶中已收集满二氧化碳的方法是________。
(2)资料:酸能使紫色石蕊试液变红。取一朵用紫色石蕊溶液染成紫色的干燥小花,将小花的一半用水喷湿,放入装置C中,可观察到的实验现象是________,此现象说明CO2能和水反应生成酸。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学实验兴趣小组为了测定某纯碱样品(只含有Na2CO3、NaCl)中Na2CO3的质量分数。取5g样品,往其中加入一定质量的稀盐酸,产生气体的质量与所加稀盐酸的质量变化如图,试计算:
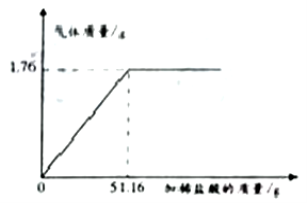
(1)其产生______g二氧化碳。
(2)该纯碱样品中Na2CO3的质量分数。
(3)求恰好完全反应时所得溶液的质量分数?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。试根据题目要求,回答下列问题:
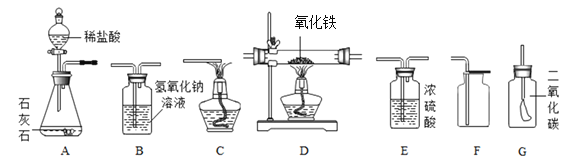
(1)欲在实验室中制备并收集干燥的二氧化碳气体。
①所选仪器的连接顺序为_________________(填写仪器序号字母)。
②仪器A中,发生反应的化学方程式为_____________________。
③若向G装置中倒入适量澄清石灰水,迅速用预先绑有小气球的橡皮塞塞紧,振荡,观察到的气球出现的现象是_______________________。
(2)欲用混有少量二氧化碳的一氧化碳气体还原氧化铁,所选仪器的连接顺序为:混合气体→D→B→C。进行实验时,D装置玻璃管中的现象是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A﹣H 是初中化学常见的物质,其相互转化关系如图所示,其中 A 是人体胃液中帮助消化的物质,B 用于改良酸性土壤。
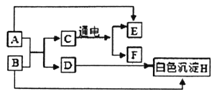
(1)D的化学式为_______。
(2) A转化为E的化学方程式_______。
(3)指出B转化为H反应的基本反应类型_______。
(4)指出物质 H 的一种用途_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】研究发现燃烧排放的气体中,CO2浓度(用体积分数表示)越高,越容易被收集。与传统的燃料燃烧方式相比,化学链燃烧具有排放CO2浓度更高,易于收集的优点。下图为利用镍元素(Ni)进行化学链燃烧的原理示意图。

(1)空气反应器中,金属镍与氧气在一定条件下发生燃烧反应,其化学方程式为______________。
(2)燃料反应器中发生的部分化学反应如下(在高温下进行):H2+ NiO![]() Ni+H2O CO + NiO
Ni+H2O CO + NiO![]() Ni+CO2 反应前后化合价发生改变的元素有________。
Ni+CO2 反应前后化合价发生改变的元素有________。
(3)与CO、H2直接在空气中燃烧相比,化学链燃烧从燃料反应器排放出的CO2浓度更 高的原因是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com