
【题目】如图所示,某同学做了有关稀盐酸的化学性质实验。
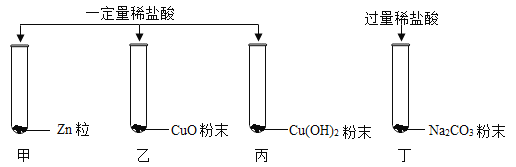
(1)甲试管中,发生反应的化学方程式为_____。
(2)四支试管,其中_____试管中的固体一定全部溶解。
(3)实验后将甲、乙、丙试管中的所有物质都倒入一个空烧杯中;稍后将丁试管中的物质倒入此烧杯中,有气泡产生。则:此气泡的气体物质是_____静置后,烧杯内上部的澄清液中的溶质一定含有_____。
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】A、B为初中化学中常见的物质,均由相同的两种元素组成。它们之间的转化关系如图所示。请根据下列描述解答相关问题:
![]()
(1)若A、B均为气体,且B有剧毒。则B物质的名称为_____;请写出A→B的化学反应方程式_____;
(2)若A、B均为无色液体,且A能产生使带火星的木条复燃的气体。则A→B的化学方程式为_____,该反应属于_____反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象中有关量的变化趋势与对应叙述关系正确的是( )
A. 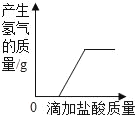 向一定质量表面生锈的铁片中滴加盐酸至过量
向一定质量表面生锈的铁片中滴加盐酸至过量
B. 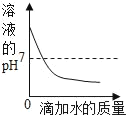 向一定质量的稀硫酸中滴加水
向一定质量的稀硫酸中滴加水
C. 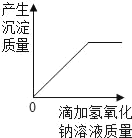 向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液
向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液
D. 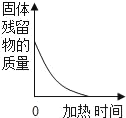 加热高锰酸钾
加热高锰酸钾
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校社会大课堂活动组织同学们走进了污水处理厂。

(1)参观污水的第一道处理工序时,现场弥漫着难闻的气味,同学们不禁掩住口鼻。从微粒的角度说明能闻到气味的原因是________。
(2)污水的第一道处理工序是经过格栅,格栅是带有规则分布的方形网格,其作用是_______。
(3)二次沉淀池的主要作用是分离出活性污泥。活性污泥的作用是利用微生物将污水中的一些有害物质在氧气的作用下经过生物降解转化为沼气。沼气(主要成分为甲烷)可作为能源使用。沼气燃烧的化学反应方程式为____。
(4)某工厂在排放含硫酸的酸性废水时用氢氧化钠进行处理,其反应的化学方程式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据KNO3、NaCl两种物质的溶解度曲线,回答下列问题:

(1)20℃时,KNO3的溶解度约为_____g。
(2)在10℃时,将25gKNO3放入100g水中,充分搅拌后,所得溶液中溶质的质量分数为_____。
(3)KNO3溶液中混有少量的NaC1,要得到较纯净的KNO3,提纯过为:蒸发浓缩、_____,再过滤。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取12g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图
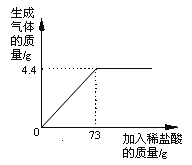
(1)纯碱恰好完全反应时,生成CO2的质量为 g
(2)计算该样品中含杂质的质量分数是多少?(计算结果保留一位小数,下同)
(3)计算当盐酸与纯碱恰好完全反应时,所得溶液的溶质质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人体缺乏维生素C(简称Vc)可能患坏血病,如图为某种“维生素C”说明书的一部分,请回答:

(1)“Vc”属于_____(填“有机”“无机”)化合物。
(2)“Vc”中碳氢氧原子的个数比是_____。
(3)“Vc”中含量最高的是_____元素。
(4)若正常成年人每天最低需要补充“Vc”60mg时,这些“Vc”完全由图中“维生素C”来补充时,则每次至少服用_____片。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答:
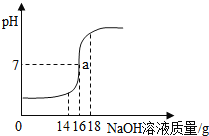
(1)a点溶液中大量存在的离子有_____;
(2)计算稀盐酸中溶质的质量分数_____
(3)当恰好完全反应时,所得溶液的溶质质量分数?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面小文章,回答问题。
氢气在通常状况下,是一种无色无味、难溶于水、在相同条件下密度最小的气体。它在空气中能安静的燃烧,产生淡蓝色的火焰。氢气常在实验室被使用,如它能和氧化铜反应,将氧化铜还原成铜,并生成水。氢气被人们所喜爱,因为它有着很多优点。如资源丰富(以水为原料制取)、燃烧产物是水(无污染)、燃烧放出热量多等等。
(1)试想,如果在实验室制取氢气,应用什么方法收集?_____、
(2)写出所有文中出现的反应的化学方程式。_____、
(3)根据文中信息,写出利用氢气物理性质和化学性质的用途各一条。_____、_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com