钢铁是人们日常生活中不可缺少的材料,厨具、建筑物中都大量使用了金属材料.
(1)以磁铁矿(主要成分为Fe3O4)为原料炼铁的化学方程式为________.
(2)全世界每年因生锈损失的钢铁约占世界钢铁年产量的1/4,这给人类带来了巨大的损失.现有一批铁质螺丝钉生锈,请写出用化学方法除锈的化学方程式及你的防锈做法.
(3)亮亮同学用稀盐酸和另一种溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的.请回答下列问题:
①亮亮所用的另一种溶液是________.
②说明Mg比Fe活泼的实验现象是________.
③说明Cu比Ag活泼的实验现象是________.
(4)北京烤鸭是具有世界声誉的北京著名菜式,食用时配大葱、甜面酱、黄瓜和薄饼.其中所含的营养素有哪些?(写出两种即可)
(5)我国在金属冶炼方面有着悠久的历史,南北朝时期就开始冶铸黄铜.黄铜是由铜和锌组成的,可以用来制造机器、电器零件及日用品.现为测定某黄铜样品中铜的含量,取该黄铜样品10g,放入100g的稀盐酸中,恰好完全反应.此时烧杯内各物质的总质量为109.8g.试计算:该黄铜样品中铜的质量分数.
解:(1)四氧化三铁和一氧化碳反应生成铁和二氧化碳,故(1)答案:Fe
3O
4+4CO

3Fe+4CO
2(2)氧化铁和稀盐酸反应生成氯化铁和水;防止铁生锈的原理是防止铁和水、氧气同时接触,方法很多只要符合防锈的原理即可.故(2)答案:
Fe
2O
3+6HCl=2FeCl
3+3H
2O 可在铁制品表面刷漆
(3)运用稀盐酸首先可验证镁比铁活泼,铁比铜银活泼,因为稀盐酸和铁镁能反应生成氢气而铜银与稀盐酸不反应不产生氢气,且镁比铁产生氢气的速度快,但不能验证铜和银的金属活动性,利用在金属活动顺序表中前面的金属能把后面的金属从它的化合物的溶液中置换出来,故答案:①CuSO
4溶液(合理即可)
②Mg与稀盐酸反应速度比Fe与稀盐酸反应速度快(,合理即可)
③Ag放在CuSO
4溶液中无现象
(4)人体所需的六大营养素包括蛋白质、糖类、脂肪、维生素、水和无机盐,蛋类食品中蛋白质含量较高,蔬菜中维生素含量较高,故(4)答案:蛋白质、维生素(合理即可)
(5)黄铜中锌和稀盐酸反应生成氢气,铜和稀盐酸不反应,故反应前后物质总质量减轻就是因为生成了氢气,首先根据质量守恒定律求出生成的氢气质量再根据锌和稀盐酸反应生成硫酸锌和氢气计算出锌的质量,即可求出铜的质量分数.故答案:
解:根据质量守恒定律可知:
生产氢气的质量为:10g+100g-109.8g=0.2g
设10g黄铜样品中含锌的质量为x
Zn+2HCl=ZnCl
2+H
2↑
65 2
x 0.2g
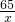
=
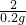
x=6.5g
黄铜样品中铜的质量分数为:
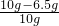
×100%=35%
答:该黄铜样品中铜的质量分数为35%.
分析:(1)运用一氧化碳的还原性解答本题.
(2)运用酸能和金属氧化物反应的性质解答.
(3)运用金属和酸、盐的反应解答比较金属的活动性顺序.
(4)运用六大营养素的知识解答.
(5)锌和稀盐酸反应的化学方程式,同时铜和稀盐酸不反应解答该题.
点评:主要考查了对金属活动性顺序的实验探究,掌握住金属和酸、盐反应,培养学生对知识的灵活应用,考查学生分析问题和计算能力.

 3Fe+4CO2
3Fe+4CO2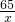 =
=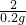
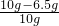 ×100%=35%
×100%=35% 

 名校课堂系列答案
名校课堂系列答案