
某气体完全燃烧,产物中有二氧化碳,则该气体组成中
A.一定含有碳
B.一定含有氧
C.一定含有碳和氧
D.一定含有碳、可能含有氧
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:初中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:初中化学 来源: 题型:

| 现象 | 结论 |
| ①.装置A质量增加,装置B质量无变化 | 猜想 猜想Ⅰ 猜想Ⅰ 成立 |
| ②.装置A质量 无变化 无变化 ,装置B质量增加 | 猜想Ⅱ成立 |
| ③.装置A质量增加,装置B质量 增加 增加 | 猜想Ⅲ成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:

| 实验事实 | 数据分析及结论 |
| 1.8g葡萄糖完全燃烧后,D装置增重1.08g,E装置增重2.64g | 数据分析:1.8g葡萄糖含有C元素 0.72 0.72 g、H元素0.12 0.12 g结论:葡萄糖含有C、H、O三种元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
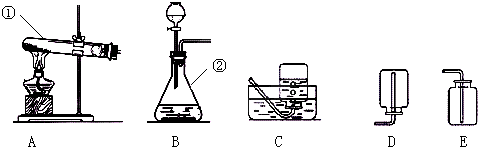
| ||
| ||
| ||
| ||
| 实验操作步骤 | 实验现象 | 实验结论 |
| ①取样品于试管中,加入适量水,充分振荡后静置并滴加几滴无色酚酞 ②或取样品于试管中,加入适量的稀盐酸 |
①试管中的液体呈红色 ② 没有气泡冒出 没有气泡冒出 |
①样品中含有: 氢氧化钙 氢氧化钙 ②样品中不含有碳酸钙. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com