
【题目】工业盐酸中通常溶有少量的FeCl3而呈黄色,小红进行了如下实验:取一定质量该工业盐酸,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示。请回答下列问题:
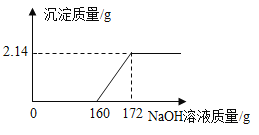
(1)FeCl3与NaOH恰好完全反应时,生成沉淀的质量是 g。
(2)所用NaOH溶液的溶质质量分数是多少?
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】绿水青山,就是金山、银山,化学绿色化是我们共同的责任。
①垃圾分类:剩饭、剩菜属于_____(填“干垃圾”或“湿垃圾”);
②植物光合作用可表示为:6H2O+6CO2 X+6O2,该反应涉及的物质中,造成温室效应的气体是_____,其中X的化学式是_____,X物质类别属于_____(填“酸”、“碱”、“盐”、“氧化物”或“有机物”)。
X+6O2,该反应涉及的物质中,造成温室效应的气体是_____,其中X的化学式是_____,X物质类别属于_____(填“酸”、“碱”、“盐”、“氧化物”或“有机物”)。
③酒精(C2H5OH))是杀灭新型冠状病毒的主要消毒剂之一,其摩尔质量为_____,0.1mol酒精约含_____个氢原子,含碳元素的质量是_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在密闭容器中放入甲、乙、丙、丁四种物质,一定条件下发生化学反应,一段时间后,测得相关数据如图所示,下列说法正确的是( )
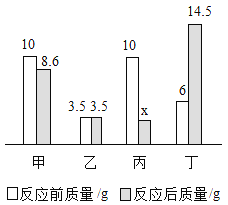
A.x=3.1B.该反应中甲、丁的质量变化比为14:85
C.该反应属于分解反应D.乙一定是该反应的催化剂
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室现有锌、石灰石、高锰酸钾、稀硫酸、稀盐酸及下列仪器:
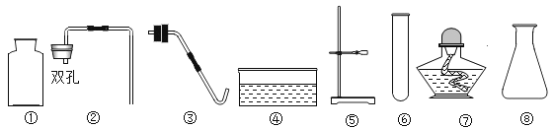
(1)仪器④的名称是_______;③中,把玻璃管插入带孔橡胶塞时,应先_______,然后对准橡胶塞上的孔稍稍用力转动,将其插入。
(2)若补充一种仪器_______(填名称),再利用上述仪器和药品一次性制取较多量的二氧化碳,应选择的仪器是_______(填序号),药品是_______。
(3)若利用棉花及上述仪器和药品制取氧气,应选择的仪器有_______(填序号),反应的化学方程式为_______。
(4)下图均为制取CO2的发生装置。其中,能“控制反应速率”的是_______(填序号,下同),能“控制反应发生和停止”的是_______。
a. 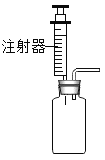 b.
b.  c.
c. 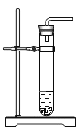 d.
d. 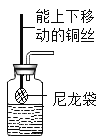
(5)利用上述药品还可制取H2,反应的化学方程式为_______;若用如图装置采用排空气法收集氢气,请在图中将导管补画完整________。
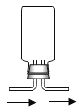
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲和乙在一定条件下反应生成丙和丁。结合微观示意图回答下列问题:
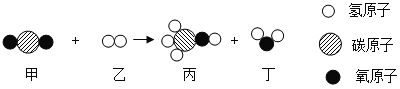
(1)丙中碳氢元素的质量比为__________。
(2)标出丁中氧元素的化合价________。
(3)该反应涉及的四种物质中有________种氧化物。
(4)该化学反应中的最小微粒是_______(选填“分子”或“原子”)。
(5)该反应的化学方程式为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合图1回答问题:
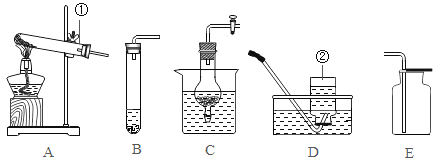
(1)仪器名称:①________________,②__________________。
(2)实验室用高锰酸钾制取并收集O2,可选用发生装置___________(选字母)和收集装置D组合,反应的化学方程式为________。
(3)实验室制取CO2的化学方程式为__________。用装置C相对于B的优点是______________;H2不可用装置E收集,理由是_______________。
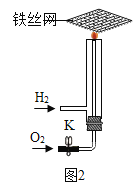
(4)氢氧焰实验:按图2所示装置进行实验
①关闭K,通入氢气,点燃(为何要先通氢气一会再点燃:________),将铁丝网放在火焰上灼烧,铁丝网只发红,不熔断。
②打开K,通入氧气,火焰更明亮,铁丝熔断,说明燃烧的剧烈程度与_________有关。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】NaCl是重要的资源,其应用与生产如下图所示。下列说法不正确的是
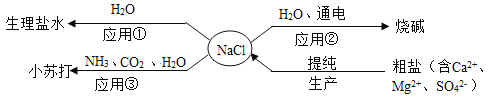
A.应用①操作的主要步骤为:计算、称量、溶解、装瓶、贴标签
B.应用②在制备烧碱的过程中,水参与了反应
C.应用③为提高产率应先通NH3,再通CO2,制备过程中还能得到一种化肥
D.生产中提纯粗盐时可依次加入过量的BaCl2、NaOH、Na2CO3溶液,再过滤、蒸发
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】MgSO47H2O 是一种重要的化工原料,某工厂以一种镁矿石(主要成分为 SiO2和 MgCO3,还含有少量 FeCO3,其它成分忽略)为原料制备 MgSO47H2O 的主要流程如图:
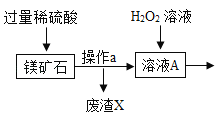
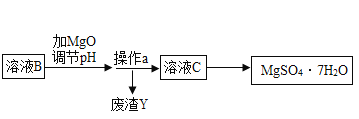
查阅资料:①SiO2既不溶于水也不溶于稀硫酸。
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Mg2+ | Fe2+ | Fe3+ |
开始沉淀时的 pH | 9.1 | 7.6 | 1.9 |
沉淀完全时的 pH | 11.1 | 9.7 | 3.2 |
请回答下列问题:
(1)MgCO3与稀硫酸发生反应的化学方程式为_________;为了让镁矿石与稀硫酸充分反应,提高原料利用率,可采取的措施为_____(填字母)。
A 将镁矿石粉碎 B 升高反应温度 C 用稀硫酸多次浸泡
(2)溶液 A中所含的溶质成分有_____;溶液 A中加入 H2O2溶液会生成 Fe2(SO4)3,该反应的化学方程式为_________。
(3)选用MgO调节pH使 Fe3+转化为沉淀,而不选用NaOH的原因是_____。加氧化镁调节后溶液的 pH范围是____ (用不等式表示)
(4)溶液C经加热浓缩、降温结晶、过滤、洗涤、低温干燥后得到 MgSO47H2O 晶体,低温干燥的目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】理科实验操作考试中,小明同学在做铝和稀盐酸反应时无意中加入硫酸铜溶液,发现铝片表面上产生气泡速率明显增快,对此他产生了兴趣。
(提出问题)硫酸铜溶液是不是此反应的催化剂?硫酸铜溶液的体积对此实验有影响吗?
(设计实验1)室温下,小明将过量、表面积相同已打磨的铝片分别加入到6份30mL10﹪稀盐酸中,并在每份中加入不同体积的硫酸铜饱和溶液,记录获得相同体积氢气的时间,从而确定产生氢气的速率。
实验混合溶液 | 1 | 2 | 3 | 4 | 5 | 6 |
硫酸铜饱和溶液/mL | 0 | 0.5 | 2.5 | 5 | 10 | 20 |
水/mL | 20 | 19.5 | 17.5 | V | 10 | 0 |
(1)上述表格中V=__________。
(2)写出铝和稀盐酸反应的化学方程式__________。
(3)定量收集氢气体积可用如图__________(填字母序号)装置。
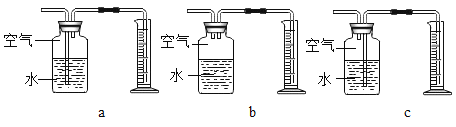
(实验现象)随着硫酸铜溶液体积的增加,产生氢气的速率先快后慢,且铝片表面附着的红色物质逐渐增加。
(结论与解释)
(4)随着硫酸铜溶液体积的增加,反应速率明显变慢可能的原因是_______________。
(5)根据实验现象小明认为硫酸铜溶液不是此反应的催化剂,其原因是______________。
(实验反思)加快铝和稀盐酸反应速率还可以采取的措施是(写一点)_____________。
(设计实验2)根据上述实验,小明认为是盐中的金属离子影响了铝和稀盐酸的反应速率;为了研究不同金属离子对反应的影响,小明同学继续实验,取过量表面积相同的铝片和30mL10﹪稀盐酸混合后加入不同的盐溶液,实验现象如下(加号越多,代表反应速率越快)。
实验 | ① | ② | ③ | ④ | ⑤ |
加入试剂0.5mL | 水 | 5﹪NaCl溶液 | 5﹪Mg(NO3)2溶液 | 5﹪FeSO4溶液 | 5﹪CuSO4溶液 |
产生气泡速率 | + | + | + | ++ | +++ |
(6)上表中,用水进行实验的目的是_______________。
(7)上述实验设计存在有缺陷,该缺陷是_____________。改进实验后,仍符合上表中的实验现象,可得到的实验结论是_________(写一点)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com