
 ��������ũ��Ʒ������ص�����ռ���Ź����г�����Խ��Խ�������ϲ������ش�
��������ũ��Ʒ������ص�����ռ���Ź����г�����Խ��Խ�������ϲ������ش����� ��1�����ݹ��˲�����Ҫ��Ͳⶨ��ҺpH�ķ�������������������к͵�ԭ�������
��2�����ݵ����ʵ��������������
��� �⣺��1��pH��ֽ�ⶨpH�ķ����ǣ���һСƬpH��ֽ���ڱ������ϣ��ò�������ͷ�ιܽ�����Һ������ֽ�ϣ��ٽ���ɫ����ֽ�����ɫ�����ն�����ֵ�����������ԣ����Լ�����Ե�ũ�ҷ��ϲ�ľ�ң���Ҫ�ɷ�̼��أ������кͣ���֤���ִ�л����˳�����У��ٽ�ֲ����������ǿ�����溦�Ϳ����������ȹ��ܣ�
�ʴ�Ϊ����һСƬpH��ֽ���ڱ������ϣ��ò�������ͷ�ιܽ�����Һ������ֽ�ϣ��ٽ���ɫ����ֽ�����ɫ�����ն�����ֵ����ľ�ң���Ҫ�ɷ�̼��أ�����л����˳�����У������溦�Ϳ�����������
��2������Ϊ�����ṩ�ḻ��Ӫ���ص����ʣ��������ǹ���ϸ���Ļ������ʣ��ǻ�����������������֯����Ҫԭ�ϣ�������̼��ˮ�ڸ������Ĵ������·�Ӧ���ɰ����Ͷ�����̼��
�÷�Ӧ�Ļ�ѧ����ʽΪ��2N2+3C+6H2O�T4NH3+3CO2��
�𰸣�ϸ���Ļ������ʣ�����������2N2+3C+6H2O�T4NH3+3CO2��
���� ���⿼���˲ⶨ��Һ���ȵķ���������кͷ�Ӧ��Ӧ���Լ��й�Ԫ��֪ʶ�Ľ���ѶȽ�С��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
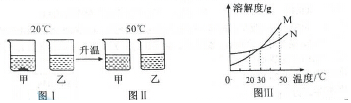
| A�� | ͼ����M��ʾ�����ʵ��ܽ������ | |
| B�� | ͼ����Һ�����������������ף��� | |
| C�� | ͼ���мס�����Һһ���Dz�������Һ | |
| D�� | 30��ʱ���ס�����Һ����������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
 θҺ�е�θ�ᣨ0.2%��0.4%�����ᣩ������ɱ��ʳ�����ϸ����ȷ��θ�ͳ����İ�ȫ��ͬʱ����θ����ø�Ļ��ԣ�����������������θҺÿ����Ҫ������������ԼΪ6.5g��7.3g��ij����ÿ�շ���������������Ϊ9.0g��Ϊ����θ����������ͼ��ʾ�����������㲢�ش�
θҺ�е�θ�ᣨ0.2%��0.4%�����ᣩ������ɱ��ʳ�����ϸ����ȷ��θ�ͳ����İ�ȫ��ͬʱ����θ����ø�Ļ��ԣ�����������������θҺÿ����Ҫ������������ԼΪ6.5g��7.3g��ij����ÿ�շ���������������Ϊ9.0g��Ϊ����θ����������ͼ��ʾ�����������㲢�ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 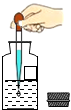 ��ȡҺ�� ��ȡҺ�� | B�� | 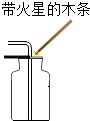 ���������Ƿ��� ���������Ƿ��� | ||
| C�� |  �����ᾧ �����ᾧ | D�� |  ��9.5mlҺ�� ��9.5mlҺ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
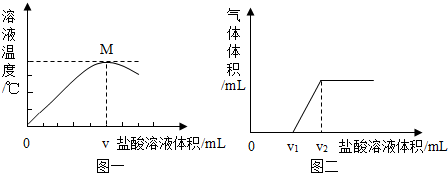
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
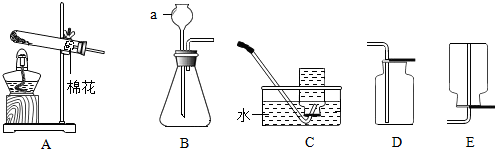
| A�� |  ̽��ȼ�յ��������� | |
| B�� | 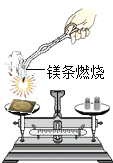 ��֤�����غ㶨�� | |
| C�� | 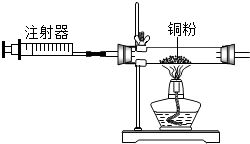 �ⶨ�����������ĺ��� | |
| D�� | 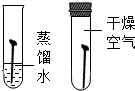 ̽������������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com