
【题目】(1)用化学用语表示:
①2个氢原子_____;
②4个铵根离子_____;
③氧化镁中镁元素的化合价为+2价_____;
④天然气的主要成分_____。
(2)如图是元素周期表中的一部分,如图是硒原子的

结构示意图。据图回答问题:
①如图中m的值为_____,n的值为_____;
②硒元素位于元素周期表中的第_____周期,硒化钠的化学式为_____。
【答案】2H 4NH4+ ![]() CH4 34 6 四 Na2Se
CH4 34 6 四 Na2Se
【解析】
(1)符号前面的数字,表示原子、分子或离子的个数;右上角的数字表示一个离子所带的电荷数;右下角的数字表示几个原子构成一个分子;元素正上方的数字表示元素的化合价。2个氢原子表示为2H,4个铵根离子表示为4NH4+,氧化镁中镁元素的化合价为+2价,表示为![]() ,天然气的主要成分是甲烷,表示为CH4;故答案为:①2H;②4NH4+;③
,天然气的主要成分是甲烷,表示为CH4;故答案为:①2H;②4NH4+;③![]() ;④CH4;
;④CH4;
(2)据图回答:①图2中m的值为34,n的值为6;②硒元素位于元素周期表中的第四周期,硒化钠的化学式为Na2Se,因为钠是+1,硒是-2价;故答案为:①34;6;②四;Na2Se;
(1)化学符号周围的数字表示不同的意义:符号前面的数字,表示原子、分子或离子的个数;右上角的数字表示一个离子所带的电荷数;右下角的数字表示几个原子构成一个分子;元素正上方的数字表示元素的化合价。2个氢原子表示为2H,4个铵根离子表示为4NH4+,氧化镁中镁元素的化合价为+2价,表示为![]() ,天然气的主要成分是甲烷,表示为CH4;
,天然气的主要成分是甲烷,表示为CH4;
(2)据图回答:①图2中m的值为34,n的值为6;②硒元素位于元素周期表中的第四周期,硒化钠的化学式为Na2Se。
本考点考查了化学式和离子符号的书写,元素符号、化学式、化学方程式等化学用语的书写是中考的重要考点之一,要加强练习,理解应用。本考点主要出现在选择题和填空题中。


科目:初中化学 来源: 题型:
【题目】草酸存在于自然界的植物中。草酸晶体(H2C2O42H2O)无色,易溶于水,于100℃开始失水,熔点 101.1℃,加热会熔化和分解(分解温度为 157℃以上),同时易升华(起始升华温度为 100℃),草酸能与氢氧化钙反应生成白色沉淀: H2C2O4+Ca(OH)2 === CaC2O4↓+2H2O 。
请回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。
①a 仪器的名称是___________________________;
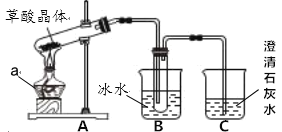
②装置 A 中试管管口向上倾斜的原因是:________;
③装置 B 的主要作用是______________;
④装置 C 中澄清石灰水变浑浊,由此可知草酸晶体分解的产物中一定有___________________________。
(2)乙组同学认为草酸晶体分解的产物中还有 CO。为进行验证,选用甲组实验中的装置 A、B 和如图所示的部分装置(可以重复选用)进行实验。
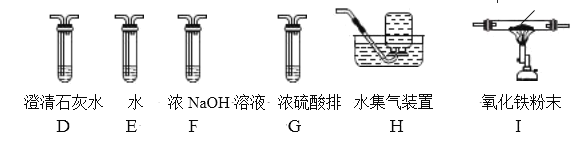
①乙组同学的实验装置依次连接的合理顺序为:
A→B→(___________)→(____________)→(_________________)→I→D→H。
②装置 I 中盛有的氧化铁发生了颜色变化,欲证明草酸晶体分解的产物中有 CO, 乙组同学需要两次使用装置 D,第一次 D 中现象__________________,第二次D 中现象___________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铜是Zn以主要添加元素的铜合金。黄铜渣中约含Zn7%、ZnO31%、Cu50%、CuO5%,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水,不参与反应):
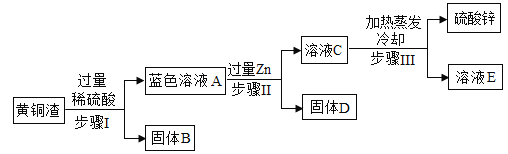
(1)溶液A中的金属阳离子有_____(填化学式)。
(2)步骤Ⅰ、Ⅱ、Ⅲ中包含的操作都要用到的玻璃仪器是_____。
(3)溶液A的质量_____(填“大于”、“小于”或“等于”)溶液C的质量。
(4)写出步骤Ⅱ中的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自然界的水里含有许多杂质,可以综合运用不同的方法进行净化。
(1)在实验室中,去除浑浊的天然水中的泥沙,主要步骤依次是:
①取大半烧杯的浑浊天然水,加入3药匙明矾粉末,明矾的作用是:_________________;搅拌溶解后,静置。
②制作过滤器的过程如图所示,其正确操作顺序为:_______________(填序号)。
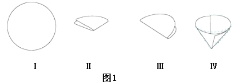
③过滤后得到澄清透明的水,该水是_______(填“纯净物”或“混合物”)。
④举出一个生活中应用过滤原理的实例_________________。
(2)取(1)中过滤后的水进行蒸馏,如图所示。连接好各部位,检查装置气密性的方法是:________。
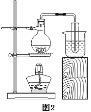
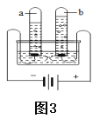
(3)取(2)中得到的纯水进行分解实验,如图所示。实验过程中,b试管产生的气体是____。写出电解水的反应方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】表中的装置制取气体(制取时将装置中的固体与液体混合)。下表为气体的制取的装置和反应的化学方程式
制取气体的装置 | 固体M | 溶液N | 制取的气体 | 反应的化学方程式 |
| 大理石 | _______。 | CO2 | __________; |
锌粒 | 稀硫酸 | ________; | __________; |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一包氯化钡和氯化钠的固体混合物32.5g,完全溶于141.2g水中,向其中逐滴加入碳酸钠溶液,反应过程中生成沉淀等质量与所加碳酸钠溶液质量的关系如图所示.计算:
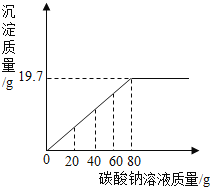
(1)所用碳酸钠溶液的溶质质量分数______;
(2)恰好完全反应时,所得溶液的溶质质量分数______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸在工业上有着重要的用途。
I.以黄铁矿(主要成分为FeS2)为原料生产硫酸的原理及工艺流程可简示如下:FeS2![]() SO2
SO2![]() H2SO4
H2SO4
(原理)
(工艺流程)
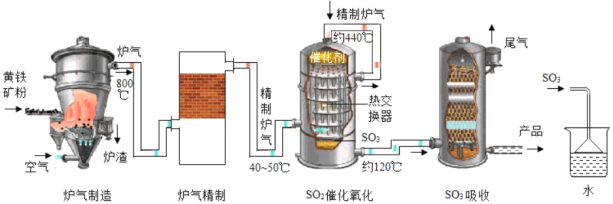
(1)黄铁矿是_____(填“纯净物”或“混合物”)工业生产过程中将矿石粉碎的目的是_____。
(2)在吸收装置中,液体由上而下形成喷雾状的目的是_____。
(3)在实验室模拟制硫酸时用如图装置吸收三氧化硫,除了达到与工业上相同的目的外,还可能考虑的因素是_____。
(4)工业上常用石灰乳来吸收尾气中的二氧化硫,请写出反应的化学方程式_____。(提示:生成物有一种是CaSO3)
II.黄铁矿锻烧后的另一种产物是铁的一种氧化物,其中铁氧质量比为7:3,则其化学式为_____。该物质可用来生产氯化铁晶体。氯化铁也是常用的净水剂之一,相比于明矾,其作为净水剂的优点是_____。
III.实验室中常用浓硫酸来配制稀硫酸。实验室用密度为1.84g/cm3、溶质质量分数为98%的浓硫酸来配制500g 20%,需要水_____g.溶解时,应_____,并用玻璃棒不断搅拌。该实验中还需用到的玻璃仪器有烧杯、量筒、_____。请写出稀硫酸的一种用途_____。
IV.某化工厂以黄铁矿为原料产生硫酸。如果该厂生产98%的浓硫酸100t,不考虑其他各生产阶段的物料损失,需要含FeS260%的矿石质量为多少吨?(写出计算过程)________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】尿素[化学式CO(NH2)2]是一种重要的氮肥,在土壤中不残留有害物质,长期施用没有不良影响。硝铵(化学式NH4NO3)也是一种常用的氮肥。
(1)尿素分子中碳、氢、氧、氮的原子个数比为_____________
(2)尿素的含氮量_____________硝铵的含氮量;(填“>”“<”或“=”)
(3)计算多少质量的硝铵中含有30g氮元素__________(算结果精确到0.1)。
(4)计算多少质量的尿素与80g硝铵中的含氮量相当__________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图中A、B、C、D、E、F分别表示六种物质,B、C、D、F分别属于酸、碱、盐、氧化物四种类别中的一种,A是目前世界年产量最高的金属,B是可溶性银盐,D与E发生的反应属于中和反应(图中用“﹣”或“︵”表示两种物质之间能发生化学反应,用“→”或“![]() ”表示一种物质可转化为另一种物质,部分反应物和生成物及反应条件已略去,图中各部分反应需在溶液中进行)。下列说法不正确的是( )
”表示一种物质可转化为另一种物质,部分反应物和生成物及反应条件已略去,图中各部分反应需在溶液中进行)。下列说法不正确的是( )
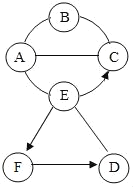
A. D可能是Ca(OH)2
B. E转化为F发生反应的化学方程式可以是2NaOH+H2SO4═Na2SO4+2H2O
C. 上述反应中涉及了四种基本反应类型
D. B与C发生反应的实验现象是有白色沉淀生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com