
【题目】人类历史发展的不同阶段曾以不同金属材料的使用作为标志。

(1)金、银在自然界有单质形式存在,说明它们的化学性质都___________。
(2)在生产生活实践中人类逐渐掌握多种金属的技术。
①比较两种铁矿石磁铁矿(主要成分Fe3O4) 和菱铁矿(主要成分FeCO3), 从化学的角度分析“磁铁矿作炼铁原料更具优势”,其原因是___________。
②近代工业上采用电解熔融氧化铝(Al2O3)的方法冶炼铝,Al2O3分解后得到两种单质,该反应的化学方程式为____________。
(3)钛和钛合金是21世纪的重要的金属材料,钛合金制品放在海水中数年取出后仍光亮如新,是因为其____ (填序号) 非常好。
A 可塑性.
B 机械性能
C 抗腐蚀性能
(4)铁在潮湿的空气中反应生成疏松的铁锈,铁锈的主要成分是__________(填化学式)。
(5)利用“活泼金属”可以制得H2,H2可用作汽车能源,若推广应用于汽车产业,则需要综合考虑的因素有________(填序号)。
a 金属原料的成本
b 生产过程中的能源消耗和污染
c 金属的回收利用
【答案】不活泼 四氧化三铁中铁元素含量高于碳酸亚铁 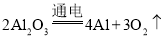 C Fe2O3 abc
C Fe2O3 abc
【解析】
电解熔融氧化铝生成铝和氧气,以单质形式存在的金属说明化学性质不活泼。
(1)以单质形式存在的金属说明化学性质不活泼,金、银在自然界有单质形式存在,说明它们的化学性质都不活泼。
(2)①要冶炼金属,金属元素含量高,产量也比较高,故原因是四氧化三铁中铁元素含量高于碳酸亚铁。
②电解熔融氧化铝(Al2O3)的方法冶炼铝,Al2O3分解后得到两种单质为铝和氧气,反应的化学方程式为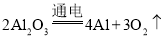 。
。
(3)钛合金制品放在海水中数年取出后仍光亮如新,说明抗腐蚀性能力强,故选C。
(4)铁锈是铁和氧气和水生成的,主要成分为氧化铁,化学式为Fe2O3。
(5)推广应用于汽车产业,则需要综合考虑的因素有成本、能源、回收问题,故选abc。


科目:初中化学 来源: 题型:
【题目】如图所示,向小烧杯中通入 CO2,烧杯内 a、c 为湿润的紫色石蕊试纸,b、d 为干燥的紫色石蕊试纸,烧杯外放一只点燃的短蜡烛。
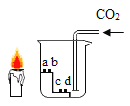
(1)能说明“CO2可与水发生反应”的现象是_______。
(2)下列说法正确的是_______(填字母序号)。
A试纸 c 比 a 先变色,说明 CO2密度大于空气
B一段时间后,蜡烛的火焰逐渐变小至熄灭,可证明 CO2密度大于空气
C若将短蜡烛放在烧杯内,蜡烛熄灭同样可证明 CO2密度大于空气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在研究酸和碱的化学性质时,同学发现稀 H2SO4 与 NaOH溶液混合后无明显现象产生,于是设计并完成了如下实验方案
方案一:测定稀H2SO4与NaOH溶液混合前后的pH。
(1)将pH试纸伸入某 NaOH溶液中测定NaOH溶液的 pH,测得 pH_____7(选填“大于”“等于”或“小于”);
(2)将一定量的稀 H2SO4加入该 NaOH溶液中,混合均匀后测定其 pH,pH=7
方案二:向盛有 NaOH溶液的烧杯中先滴加酚酞试液,后滴加稀硫酸,观察到溶液由红色变成无色
结论:稀 H2SO4与 NaOH溶液发生了化学反应,反应的化学方程式为:_____;上述实验操作中错误的是_____
(3)甲酸(HCOOH)是一种具有挥发性的酸,甲酸在热的浓硫酸中会分解生成两种氧化物:CO和_____(写化学式)如图是制取CO,用CO还原氧化铁并检验气体产物,同时收集尾气中的CO的实验装置
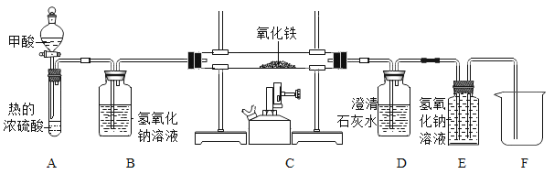
①写出C装置内玻璃管中发生反应的化学方程式:_____
②若没有B装置,则不能达到检验气体产物的目的,原因是什么_____?
③E装置可起到收集 CO的作用,实验结束时,E中有部分溶液进入到F烧杯中,请设计实验证明该溶液溶质的成分中含有NaOH,写出实验步骤、现象和结论_____
(4)工业上冶炼 150吨含杂质为 2%的生铁,需要含杂质20%的赤铁矿石多少吨___?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是宝贵的自然资源。
(1)河水经处理后可用作城市生活用水,自来水厂净水的过程中不包括的净水方法是____。
a 沉降 b 吸附 c 蒸馏 d 消毒
(2)河水中若含有难溶性杂质,可以通过过滤的方法除去。用下图装置对河水水样进行过滤,下列关于过滤的说法中正确的有____(填字母)。
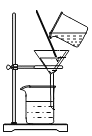
a 用玻璃棒引流
b 滤纸边缘高出漏斗
c 漏斗下端尖嘴未紧靠烧杯内壁
d 将滤纸湿润,使其紧贴漏斗内壁
e 用玻璃棒在漏斗中轻轻搅动以加快过滤速度
f 利用过滤操作,可以将氯化钠从氯化钠溶液中分离出来
(3)若要检验过滤后的液体是否为硬水,可以加入_____,搅拌后,观察现象。
(4)保护水资源是我们义不容辞的责任。下列做法不合理的有_____(填字母)。
a 严格监管化肥和农药的使用 b 不间断地放水洗衣服
c 积极探索污水处理的新技术 d 抑制水中所有动、植物的生长
(5)在盛有水的烧杯中加入一定量硝酸铵,形成溶液过程中,温度会_____(选填“升高”“降低”或“不变”)。
(6)水中加入洗涤剂能洗掉餐具上的油污,这是利用了洗涤剂的_____作用。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法不正确的是( )
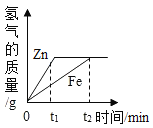
A.t1时,产生氢气的质量锌比铁大
B.t1时,产生氢气的速率锌比铁大
C.t2时,参加反应锌的质量与铁相同
D.t2时,锌、铁消耗的盐酸质量相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图像分别对应四个变化,其中正确的是()
A. 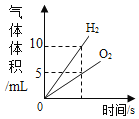 将水通电一段时间
将水通电一段时间
B.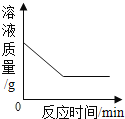 向一定量的硝酸银溶液中插入铜丝
向一定量的硝酸银溶液中插入铜丝
C. 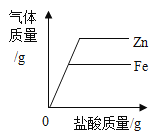 分别向等质量的锌、铁中滴加等质量分数的稀盐酸
分别向等质量的锌、铁中滴加等质量分数的稀盐酸
D.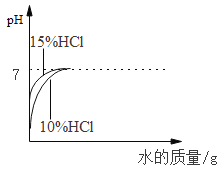 分别向等质量的溶质质量分数为15%、10%的 盐酸中不断加水
分别向等质量的溶质质量分数为15%、10%的 盐酸中不断加水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】课本第二单元课后作业中有“寻找新的催化剂”的探究内容,实验中学探究小组据此设计了如下探究方案。
[提出问题]红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
[实验探究]
实验步骤 | 实验现象 | 实验结论及解释 |
Ⅰ. | A中无明显现象,B中产生大量能使带火星木条复燃的气体 | ①产生的气体是_ ②___ |
II.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ①又产生大量能使带火星木条复燃的气体 ②滤渣质量等于ag | 红砖粉末的__在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
Ⅲ. | 两试管中均产生气泡且 __ | 红砖粉末的催化效果没有二氧化锰粉末好 |
[拓展应用]
己知CuSO4也可作为过氧化氢分解的催化剂。向101g 一定溶质质量分数的过氧化氢溶液中加入2gCuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气__g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室利用下列装置可制取多种气体。
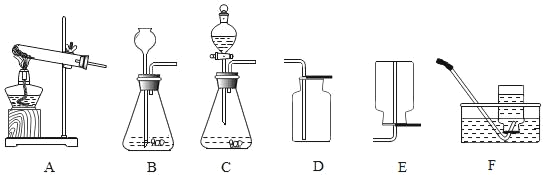
(1)要制取氧气,应选择上述装置中的_____(填序号),仪器组装后必须进行的一项操作是_____,所发生反应的化学方程式是_____,该反应属于基本反应类型中的_____。
(2)若需用碳酸钠粉末与稀盐酸反应制得二氧化碳,但反应剧烈,为便于操作,可选用上述装置中_____(填序号)来完成。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某矿石主要成分是 MgO,含少量的 Fe2O3、CuO 和 SiO2杂质。用该矿石制备Mg(OH)2的工艺流程简图如图:
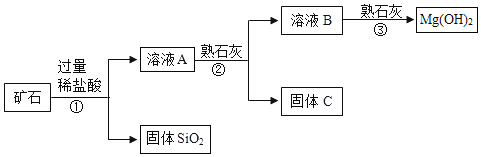
已知氢氧化铜、氢氧化铁和氢氧化镁均是沉淀,请回答下列问题:
(1)步骤①和步骤②均用到的操作是__________,需要的玻璃仪器有烧杯、漏斗和_____________。
(2)溶液 A 中所含的阳离子有 Fe3+、Cu2+、Mg2+和 __________(填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的 pH 见下表:
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的 pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的 pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的 pH 范围为_______________;固体 C 中所含固体成分的化学式为______________;该步骤②中所涉及的中和反应的化学方程式是______________。
(4)步骤③制取 Mg(OH)2的化学方程式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com