
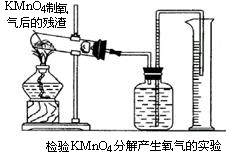
 由实验测知:取3.5gKMnO4晶体加热到220°C,分解放出的氧气多于按下式计算的理论量.按下式计算的理论量为放出氧气0.354g,2KMnO4
由实验测知:取3.5gKMnO4晶体加热到220°C,分解放出的氧气多于按下式计算的理论量.按下式计算的理论量为放出氧气0.354g,2KMnO4
| ||


科目:初中化学 来源: 题型:
| 实验序号 | 甲 | 乙 | 丙 |
| 混合物质量(g) | 9.20 | 15.7 | 27.6 |
| 生成CO2的质量(g) | 4.4 | 6.6 | 6.6 |
| (ⅰ) | (ⅱ) | (ⅲ) | |
| A的组成 | NaHCO3和MgCO3 NaHCO3和MgCO3 |
KHCO3和CaCO3 KHCO3和CaCO3 |
不需填满 不需填满 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 (2009?贵阳)图是一瓶浓硫酸标签上的部分内容,某探究小组的同学对这瓶硫酸进行了如下探究,请你参与.
(2009?贵阳)图是一瓶浓硫酸标签上的部分内容,某探究小组的同学对这瓶硫酸进行了如下探究,请你参与.| 实验步骤 | 实验现象 | 实验结论 |
| 先用pH试纸测定稀硫酸的pH,再逐滴加入氢氧化钠溶液并不断振荡,同时测混合液的pH | pH逐渐变大, 最后pH≥7 |
稀硫酸与氢氧化钠 溶液能发生反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 图是一瓶浓硫酸标签上的部分内容,某探究小组的同学对这瓶硫酸进行了如下探究,请你参与.
图是一瓶浓硫酸标签上的部分内容,某探究小组的同学对这瓶硫酸进行了如下探究,请你参与.| 实验步骤 | 实验现象 | 实验结论 |
| 先用pH试纸测定稀硫酸的pH,再逐滴加入氢氧化钠溶液并不断振荡,同时测混合液的pH | pH逐渐变大, 最后pH≥7 | 稀硫酸与氢氧化钠 溶液能发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com