36、溶液在生产和科研中具有广泛的应用,与人们的生活息息相关.请你结合题意回答问题.
(1)在农业生产上,我们常用质量分数为16%的氯化钠溶液选种,你能从“16%的氯化钠”中提取到的信息有(从两个角度叙述)
①
溶液的组成:氯化钠溶液中溶质是氯化钠,溶剂是水
;
②
溶质、溶剂、溶液的质量比为4:21:25
.
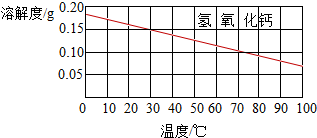
(2)在我国青海湖地区有一种说法,冬天捞碱,夏天晒盐.这里的碱是指Na
2CO
3,盐是指NaCl.从这个说法中可知碳酸钠的溶解度与温度的关系是
碳酸钠固体的溶解度随温度升高而增大
.
(3)亚硝酸钠(NaNO
2)因外观与食盐相似,经常会出现误食中毒的事件.请你根据NaNO
2和NaCl的溶解度曲线,写出鉴别NaNO
2和NaCl的方法.

20℃时,取50g固体放入盛有100g水的烧杯中,不断搅拌,若固体全溶,则为NaNO2;若固体不能完全溶解,则为NaCl
.
(4)铅蓄电池是一种电压稳定,使用方便、安全、可靠,又可以循环使用的化学电源,广泛应用于国防、交通、生产和生活中.铅蓄电池所用硫酸溶液的溶质质量分数为31%,若用98%(密度为1.84g/cm
3)的浓硫酸配制上述硫酸溶液,则浓硫酸和水的体积比约是
1:4
.
(5)酸、碱、盐在水中可解离出阴阳离子,我们现阶段所学的复分解反应的实质就是酸、碱、盐解离出的一些阴、阳离子相互结合生成难解离的水、气体或沉淀,如图是氢氧化钠溶液和盐酸反应实质的微观示意图.
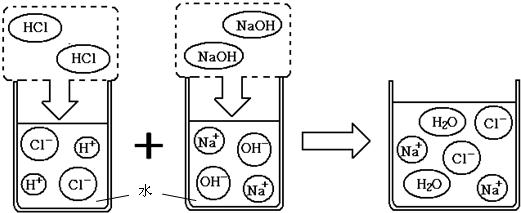
请你依据溶解性表和复分解反应实质判断下列两组物质(①硫酸钠和氯化亚铁、②碳酸钠和氢氧化钙)在水中混合后能否发生反应,若能,仿照示例在如图的圆圈中填入适当的物质或离子符号,来体现反应的实质.







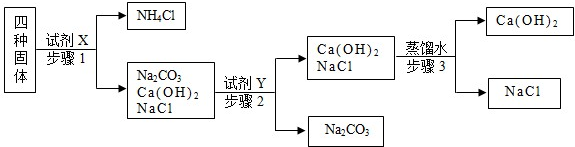
 我国有较长的海岸线,海洋资源十分丰富.
我国有较长的海岸线,海洋资源十分丰富.