【答案】
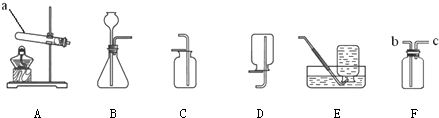
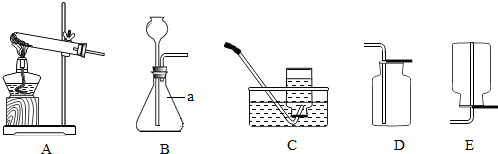
分析:(1)根据常用仪器的名称和用途解答;
(2)根据实验室用石灰石和稀盐酸制取二氧化碳应该选择的发生装置确定氧气的制法并写出反应的方程式;根据气体的密度和溶解性选择收集装置;
(3)根据实验室制取气体要求操作简单易行、生成物容易分离等选择合适的制取方法;并根据实验室制取气体,发生装置根据反应条件和药品状态做出选择,主要有“固液不需加热”和“固体加热”型两套发生装置;根据氨气的密度选择进气口;
(4)通过气体的制取进行综合比较选择选项.
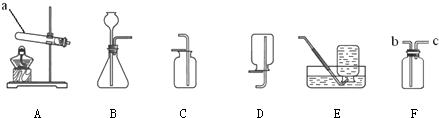
解答:解:(1)实验仪器a的名称是试管;
(2)石灰石和稀盐酸反应生成氯化钙、水和二氧化碳,反应的方程式为:CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑;反应在常温下进行,反应物为固体与液体反应,因此发生装置是B装置,该法制取氧气应该是过氧化氢溶液和二氧化锰的混合物,因此反应的方程式为:2H
2O
2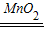
2H
2O+O
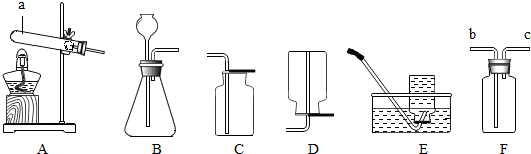
2↑;因为二氧化碳可溶于水,且密度比空气的大,因此采用向上排空气法收集;因为氧气的密度比空气大,不易溶于水,因此可以采用向上排空气法或排水法收集;F装置是一个多功能的收集装置;
(3)实验室制取气体要求操作简单易行,第一种方法产生两种气体,不易分离;第二种方法反应条件“高温高压催化剂”,操作起来难度大不宜操作,而第三种方法仅需要加热,容易操作,所以选择第三种方法制取氨气;
“氯化铵固体和熟石灰粉末在加热条件下生成氨气”,应选择“固体加热”型发生装置A装置;氨气“极易溶于水、密度比空气小”,所以进气口是短管;
(4)实验室制取气体的下列因素中:
①反应所需的条件 可以是常温或加热,因此不需要考虑;
②反应物不能有气体参加,需要考虑,因为若反应物的气体反应不完全,会使收集的气体不纯;
③反应物必须是固体不需要考虑,固体、液体均可以;
④生成物容易分离,需要考虑;
⑤生成物只能有一种不需要考虑,只要易于分离即可;
因此实验室制取气体总结出选择制取气体的原理必须考虑的是:①②④.
故答案为:(1)试管;(2)B; 2H
2O
2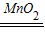
2H
2O+O
2↑ ( 或 CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑ );
C或E或F(或C或F);(3)③; A; c;(4)①②④.
点评:明确装置的选取方法并会应用知识分析和解决问题,掌握氧气、二氧化碳的实验室制取原理和和发生装置、收集方法的选择依据,以及实验室制取气体的一般原则是解题的关键.

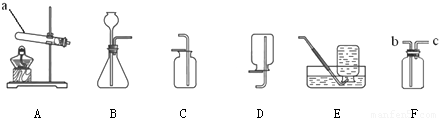
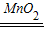 2H2O+O2↑;因为二氧化碳可溶于水,且密度比空气的大,因此采用向上排空气法收集;因为氧气的密度比空气大,不易溶于水,因此可以采用向上排空气法或排水法收集;F装置是一个多功能的收集装置;
2H2O+O2↑;因为二氧化碳可溶于水,且密度比空气的大,因此采用向上排空气法收集;因为氧气的密度比空气大,不易溶于水,因此可以采用向上排空气法或排水法收集;F装置是一个多功能的收集装置;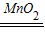 2H2O+O2↑ ( 或 CaCO3+2HCl═CaCl2+H2O+CO2↑ );
2H2O+O2↑ ( 或 CaCO3+2HCl═CaCl2+H2O+CO2↑ );

 NH3↑+H2O+CO2↑;
NH3↑+H2O+CO2↑;  2NH3;
2NH3; CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O