

| 15g |
| 15g+50g |


科目:初中化学 来源: 题型:
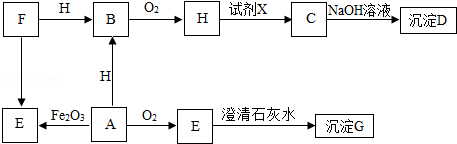
查看答案和解析>>
科目:初中化学 来源: 题型:
| A |
| △ |
| 点燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:
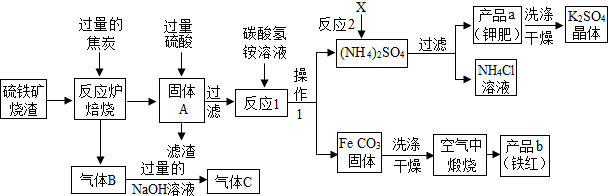
| 物质 | X | K2SO4 | NH4Cl | (NH4)2SO4 |
| 溶解度g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
| ||
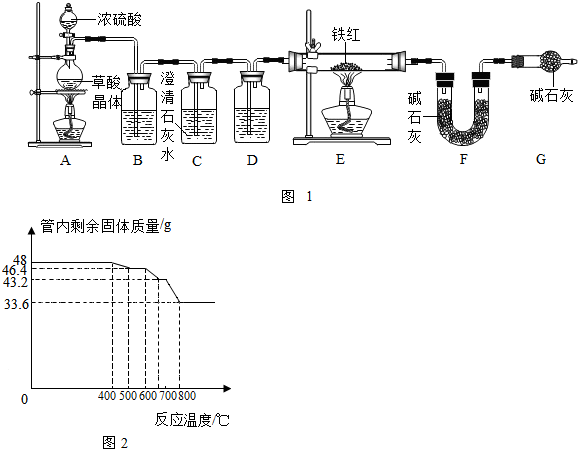
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
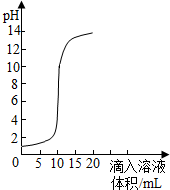 (1)向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成
(1)向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
| 选项 | 物质 | 杂质 | 除去杂质所选试剂 | 操作方法 |
| A | CO2 | CO | O2 | 点燃 |
| B | KCl | K2CO3 | 稀盐酸 | 蒸发 |
| C | Zn | Fe | 稀硫酸 | 过滤 |
| D | CaO | CaCO3 | 稀盐酸 | 蒸发 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com